Les données de génétique postnatale correspondent à l’activité 2012 des laboratoires. Elles ont été recueillies de manière spécifique en coopération avec Orphanet. Ce rapport ne comprend pas l’activité des consultations de génétique. La base de données a été figée le 27 mars 2012. Les modifications apportées après cette date n’ont pas été prises en compte.
Le rapport d’activité de génétique postnatale constitue un outil important notamment dans le cadre de la réalisation des SROS et de la mise en place du second plan maladies rares. Ce rapport unique en Europe, créé relativement récemment est en constante évolution pour s’adapter aux évolutions des pratiques.
La participation de plus de 99% des laboratoires contactés est très satisfaisante. Seuls 2 laboratoires n’ont pas rendu de rapport.
Les laboratoires de génétique postnatale
Parmi les 236 laboratoires ayant déclaré une activité à l’Agence de la biomédecine, 75 ont au moins une activité de cytogénétique y compris cytogénétique moléculaire et 181 au moins une activité de génétique moléculaire. Près de 40% des laboratoires autorisés pour la génétique moléculaire le sont uniquement pour une activité limitée. Dans cette dernière situation l’activité peut être limitée à un ou plusieurs examens de réalisation et d’interprétation généralement plus simples (tableaux POSTNATAL1 et POSTNATAL2).
Les deux cartes de la figure POSTNATAL1 montrent la répartition géographique des laboratoires sur le territoire français. Toutes les régions (hormis la Corse) possèdent au moins un laboratoire de cytogénétique constitutionnelle. La répartition de cette activité sur le territoire donne une indication sur l’organisation et l’offre de soins. En revanche, la répartition géographique de l’activité de génétique moléculaire ne donne d’information que sur l'existence de laboratoires mais en aucun cas ne peut permettre d'appréhender l'offre de soins de proximité. En effet, les prélèvements voyageant, certains laboratoires proposent un diagnostic pour l'ensemble de la France, souvent ils travaillent en réseau. Les laboratoires ayant une activité non limitée ne peuvent pas et ne doivent pas développer un catalogue complet de diagnostics car ils doivent maintenir l’expertise nécessaire à l’analyse et l’interprétation des résultats. Seule une cartographie des consultations de génétique pourrait montrer l'accès aux soins au niveau régional.
Tableau POSTNATAL1. Laboratoires autorisés pour une activité de génétique postnatale d'après les déclarations faites dans les rapports d'activité et en cours de validation par les ARS
|
2009 |
2010 |
2011 |
2012 |
Nombre de laboratoires proposant une activité de cytogénétique |
75 |
75 |
77 |
75 |
Nombre de laboratoires proposant une activité de génétique moléculaire |
182 |
188 |
186 |
181 |
avec une activité à autorisation non limitée |
101 |
108 |
107 |
110 |
avec une activité à autorisation limitée |
81 |
80 |
79 |
71 |
Nombre total de laboratoires* |
239 |
236 |
244 |
236 |
|
* Certains laboratoires proposent une activité de génétique moléculaire et de cytogénétique |
||||
Tableau POSTNATAL2. Activités pratiquées par les laboratoires de génétique moléculaire ayant une autorisation limitée
|
Nombre de laboratoires |
||
2010 |
2011 |
2012 |
|
Facteurs II et V |
43 |
36 |
35 |
Hématologie |
22 |
20 |
18 |
Hémochromatose |
16 |
14 |
16 |
Analyses de biologie moléculaire appliquées à la cytogénétique |
10 |
3 |
3 |
Pharmacogénétique |
9 |
12 |
8 |
Typages HLA |
4 |
6 |
8 |
Autre |
28 |
29 |
24 |
Répartition des laboratoires de cytogénétique et de génétique moléculaire postnatale ayant déclaré une activité de génétique postnatale sur le territoire Français
Figure POSTNATAL1. Répartition géographique des laboratoires de cytogénétique et de génétique moléculaire postnatale ayant déclaré une activité en 2012

Résumé de l’activité de génétique postnatale
Tableau POSTNATAL3. Résumé de l’activité de génétique postnatale
|
2009 |
2010 |
2011 |
2012 |
Cytogénétique |
||||
Nombre d’analyses totales |
80978 |
84925 |
84983 |
82756 |
par caryotypes |
68186 |
70997 |
71543 |
69393 |
par FISH |
12792 |
13928 |
13440 |
13363 |
Génétique moléculaire (y compris pharmacogénétique) |
||||
Nombre de diagnostics de maladies différentes |
|
|||
disponibles |
1060 |
1205 |
1282 |
1526 |
réalisés |
951 |
1024 |
1012 |
1250 |
Nombre de gènes |
|
|||
disponibles |
1143 |
1242 |
1337 |
1522 |
testés |
1042 |
1123 |
1192 |
1343 |
Nombre d’examens réalisés |
271330 |
361169 |
387059 |
416767 |
Puces |
||||
Nombre de dossiers rendus |
6596* |
13728** |
10104 |
12151 |
|
*Ce chiffre n'est pas comparable aux années suivantes car le mode de recueil était différent |
||||
L’activité des laboratoires de cytogénétique postnatale (hors puce) est stable ces trois dernières années. En 2012, 72 850 individus ont bénéficié de ce type d’examen. Avec 69 393 caryotypes réalisés en 2012, cet examen de génétique reste très pratiqué (tableau POSTNATAL3). Les analyses d’hybridations in situ (FISH) sont souvent réalisées en complément d’un caryotype, et pour une petite partie dans le cadre de la validation de résultats de puces.
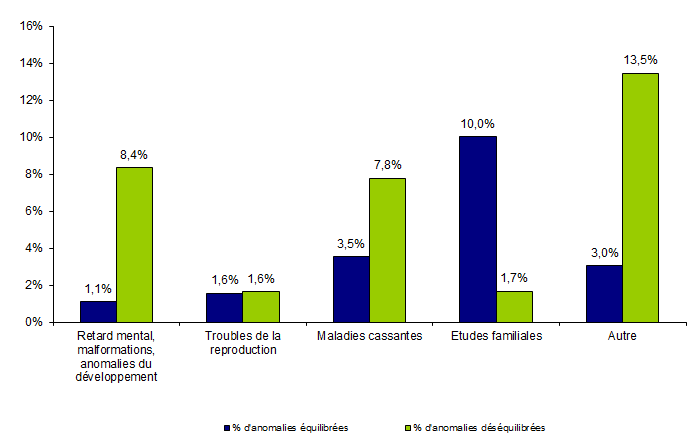
Les grands groupes d’indications sont présentés dans le tableau POSTNATAL4. Les examens de cytogénétique postnatale sont plus souvent prescrit pour expliquer un trouble de la reproduction, néanmoins le taux d’anomalies diagnostiquées pour cette indication est le plus faible (figure POSTNATAL2).
A noter que le nombre d’examen total n’est pas nécessairement égal à la somme des résultats de caryotypes probablement en raison d’échecs de culture.
En plus de ces grands groupes d’indications définis en collaboration avec les sociétés savantes de cytogénétique, l’Agence de la biomédecine recueille spécifiquement le nombre de cas de trisomies 21 diagnostiqués en génétique postnatale (tableau POSTNATAL5). Cette donnée fait partie du dispositif global de suivi du dépistage de la trisomie 21 au premier trimestre et est donc à commenter dans ce contexte (cf. rapport annuel d’activité de diagnostic prénatal). L’augmentation du nombre de diagnostics postnatals de trisomie 21 entre 2011 et 2010 n’est pas confirmée en 2012.
Tableau POSTNATAL4. Activité de cytogénétique postnatale en 2012 selon l'indication
Indications |
Techniques |
Nombre d’examens |
Nombre de résultats normaux |
Nombre d'anomalies équilibrées |
Nombre d'anomalies déséquilibrées |
Retard mental, malformation, anomalies du développement |
Caryotype |
18639 |
16883 |
202 |
1558 |
FISH |
7165 |
5406 |
183 |
1585 |
|
Troubles de la reproduction |
Caryotype |
40361 |
39078 |
627 |
656 |
FISH |
2243 |
1385 |
451 |
408 |
|
Maladies cassantes |
Caryotype |
283 |
251 |
10 |
22 |
FISH |
19 |
14 |
2 |
3 |
|
Etudes familiales |
Caryotype |
7709 |
6814 |
773 |
129 |
FISH |
3453 |
2573 |
415 |
485 |
|
Autre |
Caryotype |
2401 |
2006 |
73 |
323 |
FISH |
483 |
347 |
43 |
93 |
|
Total |
Caryotype |
69393 |
65032 |
1685 |
2688 |
FISH |
13363 |
9725 |
1094 |
2574 |
Tableau POSTNATAL5. Suivi du nombre de cas de trisomie 21 en diagnostic postnatal
|
2010 |
2011 |
2012 |
Nombre de cas de T21 diagnostiqués |
453 |
535 |
488 |
Figure POSTNATAL2. Pourcentage d’anomalies identifiées par caryotype en 2012 selon l’indication et le type d’anomalie
Activité de recherche d'une anomalie chromosomique par analyse moléculaire
Les recherches d’anomalies chromosomiques par analyse moléculaire sont des techniques aussi bien utilisées par les laboratoires de cytogénétique que par les laboratoires de génétique moléculaire.
L’organisation des différents laboratoires ou plateformes est très variable, ce qui rend compliqué le recueil de l’activité dans ce domaine. L’information qui a semblé la plus pertinente étant le nombre de patients ayant accès à un diagnostic par cette technologie, le choix a été fait d’analyser le nombre de dossiers rendus. Cette donnée correspond à un résultat diagnostique rendu au prescripteur après analyse des puces et validation de l’anomalie génétique identifiée par une autre technique (en général Fish ou PCR).
Analyses par puce
Au total, le rapport d’activité recense plus de 12 000 dossiers d’analyses par puces rendus en 2012. Ce chiffre est en augmentation de plus de 2 000 examens (+20%) par rapport à 2011 (tableau POSTNATAL3). Cette augmentation correspond à la montée en charge de l’utilisation de cet examen du fait entre autres d’une appropriation de cette technologie par les laboratoires et les prescripteurs. Avec notamment la mise en place du second plan maladies rares, cette tendance devrait se confirmer dans les prochaines années en effet, les laboratoires n’arrivent actuellement pas à satisfaire pleinement la demande.
Dans près de 95% des cas, les puces sont utilisées pour des analyses pangénomiques et non pour des analyses ciblées. L’indication majoritaire (46,4%) est « Déficience intellectuelle ou trouble des apprentissages dans un cadre syndromique».
Tableau POSTNATAL6. Examens ciblés par puce en 2012
|
Analyses ciblées par puces |
Nombre de dossiers rendus |
638 |
Nombre de dossiers positifs rendus |
234 |
% de dossiers positifs rendus |
36,7% |
Tableau POSTNATAL7. Examens pangénomiques par puce en 2012
Indications |
Nombre de dossiers rendus |
Nombre de dossiers positifs rendus |
% de dossiers positifs rendus |
Déficience intellectuelle ou trouble des apprentissages dans un cadre syndromique |
5339 |
1079 |
20,2% |
Malformations sans retard psychomoteur |
1117 |
172 |
15,4% |
Déficience intellectuelle ou troubles des apprentissages isolés |
2208 |
490 |
22,2% |
Troubles Envahissants du Développement (TED) / Autisme |
1108 |
148 |
13,4% |
Caractérisation d'une anomalie découverte au caryotype ou par une autre technique (MLPA, FISH,…) |
346 |
255 |
73,7% |
Fœtopathologie |
632 |
110 |
17,4% |
Autres |
745 |
149 |
20,0% |
Total |
11495 |
2403 |
20,9% |
Autres recherches d'anomalie chromosomique par analyse moléculaire (MLPA, QF-PCR, QMPSF…)
D’autres techniques de génétique moléculaire permettent la recherche d’anomalies chromosomiques, notamment : la MLPA (Multiplex ligation-dependent probe amplification), QF-PCR (Quantitative Fluorescence - polymerase chain reaction) et la QMPSF (Quantitative Multiplex PCR of Short Fragments). Près de 16 954 examens utilisant ces types de techniques ont été déclarés par les laboratoires en 2012. Ce chiffre est en constante augmentation depuis 3 ans (+9% entre 2011 et 2012). Une partie de ces examens est réalisée dans le cadre de validation de résultats de puces.
Activité de génétique moléculaire
En 2012, plus de 416 767 examens de génétique moléculaire ont été réalisés en France (tableau POSTNATAL3). Ils incluaient 21 700 examens de pharmacogénétique (5,2 %).
Pour identifier les maladies, nous avons décidé de nous baser sur la classification de l’encyclopédie Orphanet. Ainsi peuvent être comptabilisées comme deux pathologies distinctes deux formes d’une même maladie enregistrées sous deux numéros ORPHA différents.
Génétique des maladies
En 2012, les laboratoires français avaient développé des examens diagnostiques pour 1 442 maladies différentes (selon la classification Orphanet). Ces maladies étant dans leur grande majorité rares, voir extrêmement rares, 1 187 maladies ont réellement fait l’objet de recherche diagnostique. Ces examens ont concerné un peu plus de 1 300 gènes différents (tableau POSTNATAL8). Au total, environ 323 100 personnes ont eu un examen de génétique moléculaire, qu’il s’agisse de cas index (personne symptomatique chez qui on fait le diagnostic) ou d’apparentés.
Deux indications, « hémochromatose » et « thrombophilie non rare » (2 gènes) représentent à elles seules plus de 37 % des examens réalisés en 2011 (tableau POSTNATAL8). Si en volume ce chiffre est important, il ne faut pas oublier qu’en charge de travail l’analyse de gènes complexes est beaucoup plus chronophage et coûteuse que ces deux examens. L’hémochromatose, seul examen de génétique postnatale à la nomenclature est proposée par 57 laboratoires différents (tableau POSTNATAL9). La recherche de « thrombophilie non rare », examen de susceptibilité, n’est pas à la nomenclature. Il représente à lui seul plus de 27,5% du volume d’activité des laboratoires de génétique moléculaire (tableau POSTNATAL9).
La liste des 50 examens les plus réalisés en France (tableau POSTNATAL10) montre la présence de plusieurs maladies pour lesquelles les gènes impliqués sont des gènes de susceptibilité. Une réflexion globale sur l’intérêt de tels examens devra être menée. A titre d’exemple plus de 83 000 (21%) examens ont portés sur des gènes du HLA en 2012 (hors indication de greffe).
Les laboratoires français ont développé entre 1 et 100 diagnostics de maladies, mais près de 30% d’entre eux ne proposent qu’un ou deux tests différents (figure POSTNATAL4).
Les maladies génétiques sont très majoritairement rares voir très rares. Développer des examens diagnostiques pour ces dernières peut se révéler très complexe. Ainsi, les laboratoires se sont généralement spécialisés, 98 laboratoires sont seuls à proposer le diagnostic d’une (ou de plusieurs) maladie(s) en France. Au final, 882 maladies (~ 60 %) ne sont diagnostiquées que dans un seul laboratoire (tableau POSTNATAL11).
Certaines maladies sont plus fréquemment proposées au diagnostic. Dans la majorité des cas il y a une relation entre le nombre de laboratoires offrant un examen et le nombre d’examens totaux réalisés. Une analyse de niveau 1 consiste en la recherche des mutations les plus fréquentes dont la causalité pour la maladie étudiée est clairement démontrée. La technique utilisée est généralement simple et souvent basée sur des dispositifs spécifiquement établis pour une recherche ciblée. En conséquence, le résultat d’une analyse de niveau 1 est le plus souvent binaire et toutes les mutations ne sont généralement pas étudiées. Une analyse de niveau 2 consiste en l’analyse exhaustive du gène, la technique peut être simple ou complexe. Toute technique de balayage pour rechercher des mutations inconnues rentre dans ce cadre. Pour ce faire, le laboratoire devra assurer notamment la prise en charge d’échantillons d’autres laboratoires lorsque les analyses de niveau 1 n’ont pas permis de mettre en évidence de mutation et si le contexte clinique le justifie, la veille technologique et scientifique, la participation à l’organisation du contrôle de qualité, le lien avec un centre de référence de la maladie s’il existe. Le laboratoire réalisant une analyse de niveau 1 est en relation avec un laboratoire de niveau 2 pour cette même analyse. Il est souhaitable que ce dernier laboratoire soit celui qui organise le contrôle de qualité (tableau POSTNATL9). Une amélioration du recueil de cette information (niveau du l’examen) par les laboratoires sera utile pour mieux appréhender le travail en réseau.
La figure POSTNATAL3 montre la fréquence des maladies par nombre d’examens pratiqués et illustre la rareté de la majorité des maladies génétique. En effet, plus d’un tiers des maladies ne sont réalisées au maximum que 10 fois dans l’année et un autre tiers entre 10 et 50 fois.
Le nombre d’examens est plus élevé que le nombre d’individus testés car pour une même maladie l’analyse de plusieurs gènes en parallèles ou successivement peut être nécessaire pour poser un diagnostic.
Tableau POSTNATAL8. Activité de génétique moléculaire postnatale (hors pharmacogénétique)
|
2010 |
2011 |
2012 |
Nombre de maladies différentes |
|
|
|
Disponibles |
1084 |
1253 |
1442 |
Réalisés |
950 |
1010 |
1187 |
Nombre de gènes différents |
|
|
|
Disponibles |
1212 |
1403 |
1504 |
Testés |
1093 |
1219 |
1323 |
Nombre d’examens réalisés |
349605 |
369051 |
395066 |
dont hémochromatose et facteur II facteur IV |
140605 |
151532 |
146852 |
Tableau POSTNATAL9. Nombre d’examens et de laboratoires pour une maladie étudiée par au moins dix laboratoires par génétique moléculaire postnatale en 2012
| Numéro ORPHA | Maladie |
Nombre de laboratoires total |
Nombre d’examens |
Nombre de laboratoires ayant effectué un examen de niveau 1 |
Nombre de laboratoires ayant effectué un examen de niveau 2 |
ORPHA64738 |
Thrombophilie non rare |
68 |
108515 |
64 |
4 |
ORPHA139498 |
Hémochromatose type 1 |
57 |
38337 |
49 |
8 |
ORPHA740 |
Syndrome de Prader-Willi |
38 |
1109 |
26 |
12 |
ORPHA586 |
Mucoviscidose |
35 |
11427 |
23 |
12 |
ORPHA908 |
Syndrome de l' X fragile |
32 |
10003 |
20 |
12 |
ORPHA1646 |
Délétion partielle de l'Y |
31 |
4154 |
23 |
8 |
ORPHA48 |
Absence congénitale bilatérale des canaux déférents |
23 |
473 |
11 |
12 |
ORPHA144 |
Cancer du côlon héréditaire non polyposique |
20 |
3977 |
3 |
17 |
ORPHA273 |
Dystrophie myotonique de type 1 |
20 |
2000 |
9 |
11 |
ORPHA676 |
Pancréatite chronique héréditaire |
20 |
2804 |
10 |
10 |
ORPHA72 |
Syndrome d'Angelman |
18 |
535 |
14 |
4 |
ORPHA145 |
Syndrome héréditaire de prédisposition au cancer du sein et de l'ovaire |
17 |
20764 |
1 |
16 |
ORPHA90635 |
Surdité neurosensorielle non syndromique autosomique dominante type DFNA |
15 |
403 |
6 |
9 |
ORPHA90636 |
Surdité neurosensorielle non syndromique autosomique récessive type DFNB |
15 |
1419 |
5 |
10 |
ORPHA232 |
Drépanocytose |
13 |
759 |
7 |
6 |
ORPHA399 |
Maladie de Huntington |
13 |
1047 |
8 |
5 |
ORPHA70 |
Amyotrophie spinale proximale |
13 |
1781 |
8 |
5 |
ORPHA357 |
Syndrome de Gilbert |
12 |
350 |
9 |
3 |
ORPHA653 |
Néoplasie endocrinienne multiple type 2 |
12 |
524 |
4 |
8 |
ORPHA848 |
Bêta-thalassémie |
12 |
552 |
2 |
10 |
ORPHA550 |
Syndrome MELAS |
11 |
893 |
5 |
6 |
ORPHA551 |
Syndrome MERRF |
11 |
504 |
5 |
6 |
ORPHA644 |
Syndrome NARP |
11 |
407 |
5 |
6 |
ORPHA825 |
Spondylarthrite ankylosante |
11 |
33983 |
8 |
3 |
ORPHA242 |
Dysgénésie gonadique complète 46,XY |
10 |
59 |
5 |
5 |
ORPHA262 |
Dystrophie musculaire de Duchenne et Becker |
10 |
1141 |
5 |
5 |
ORPHA324 |
Maladie de Fabry |
10 |
337 |
3 |
7 |
ORPHA480 |
Syndrome de Kearns-Sayre |
10 |
245 |
5 |
5 |
ORPHA619 |
Insuffisance ovarienne primaire |
10 |
628 |
3 |
7 |
ORPHA733 |
Polypose adénomateuse familiale |
10 |
761 |
3 |
7 |
ORPHA96334 |
Disomie uniparentale paternelle du chromosome 14 |
10 |
28 |
9 |
1 |
ORPHA98878 |
Hémophilie A |
10 |
726 |
4 |
6 |
Tableau POSTNATAL10. Listes des 50 indications faisant l’objet du plus grand nombre d’examens
ORPHA |
MALADIE |
Nombre d’examens |
ORPHA64738 |
Thrombophilie non rare |
108515 |
ORPHA139498 |
Hémochromatose type 1 |
38337 |
ORPHA825 |
Spondylarthrite ankylosante |
33983 |
ORPHA117 |
Maladie de Behçet |
26967 |
ORPHA145 |
Syndrome héréditaire de prédisposition au cancer du sein et de l'ovaire |
20764 |
ORPHA586 |
Mucoviscidose |
11427 |
ORPHA908 |
Syndrome de l' X fragile |
10003 |
ORPHA243377 |
Diabète sucré de type 1 |
7247 |
ORPHA2073 |
Narcolepsie-Cataplexie |
6582 |
ORPHA1646 |
Délétion partielle de l'Y |
4154 |
ORPHA144 |
Cancer du côlon héréditaire non polyposique |
3977 |
ORPHA555 |
Maladie coeliaque |
3277 |
ORPHA284130 |
Polyarthrite rhumatoïde |
3131 |
ORPHA676 |
Pancréatite chronique héréditaire |
2670 |
ORPHA29072 |
Pheochromocytome-paragangliome héréditaire |
2239 |
ORPHA618 |
Mélanome malin familial |
2070 |
ORPHA273 |
Dystrophie myotonique de type 1 |
2000 |
ORPHA247 |
Dysplasie ventriculaire droite arythmogène |
1969 |
ORPHA325 |
Déficit congénital en facteur II |
1906 |
ORPHA155 |
Cardiomyopathie hypertrophique familiale isolée |
1862 |
ORPHA70 |
Amyotrophie spinale proximale |
1781 |
ORPHA406 |
Hypercholestérolémie familiale |
1761 |
ORPHA552 |
Syndrome MODY |
1420 |
ORPHA90636 |
Surdité neurosensorielle non syndromique autosomique récessive type DFNB |
1419 |
ORPHA846 |
Alpha-thalassémie |
1293 |
ORPHA648 |
Syndrome de Noonan |
1265 |
ORPHA342 |
Fièvre méditerranéenne familiale |
1261 |
ORPHA101016 |
Syndrome de Romano-Ward |
1168 |
ORPHA262 |
Dystrophie musculaire de Duchenne et Becker |
1141 |
ORPHA739 |
Syndrome de Prader-Willi |
1054 |
ORPHA399 |
Maladie de Huntington |
1047 |
ORPHA652 |
Néoplasie endocrinienne multiple type 1 |
951 |
ORPHA53690 |
intolérance primaire au lactose |
950 |
ORPHA550 |
Syndrome MELAS |
893 |
ORPHA71529 |
Obésité par déficit du récepteur de la mélanocortine 4 |
875 |
ORPHA791 |
Rétinite pigmentaire |
849 |
ORPHA774 |
Maladie de Rendu-Osler-Weber |
842 |
ORPHA220460 |
Polypose adénomateuse familiale atténuée |
839 |
ORPHA95698 |
Hyperplasie congénitale des surrénales par déficit en 21-hydroxylase non-classique |
794 |
ORPHA803 |
Sclérose latérale amyotrophique |
762 |
ORPHA805 |
Sclérose tubéreuse de Bourneville |
762 |
ORPHA733 |
Polypose adénomateuse familiale |
761 |
ORPHA232 |
Drépanocytose |
759 |
ORPHA478 |
Syndrome de Kallmann |
749 |
ORPHA100973 |
Déficit intellectuel FRAXE |
747 |
ORPHA104 |
Neuropathie optique héréditaire de Leber |
726 |
ORPHA98878 |
Hémophilie A |
726 |
ORPHA110 |
Syndrome de Bardet-Biedl |
718 |
ORPHA275742 |
Infertilité génétique |
717 |
ORPHA91387 |
Anévrysme familial de l'aorte thoracique |
712 |
Figure POSTNATAL3. Répartition de la fréquence des maladies par nombre d’examens réalisés en 2012

Tableau POSTNATAL11. Description de l’activité de génétique moléculaire postnatale
|
2010 |
2011 |
2012 |
Nombre de laboratoires |
|||
qui n'étudient que l'hémocromatose |
3 |
2 |
2 |
qui n'étudient que la thrombophilie |
21 |
19 |
18 |
Nombre de laboratoires |
|||
qui diagnostiquent une maladie qui n'est étudiée que dans 1 laboratoire en France |
97 |
102 |
98 |
qui diagnostiquent une maladie qui n'est étudiée que dans 2 laboratoires en France |
97 |
99 |
105 |
Nombre de maladies |
|||
qui ne sont étudiées que dans 1 laboratoire en France |
665 |
810 |
882 |
qui ne sont étudiées que dans 2 laboratoires en France |
220 |
251 |
294 |
Figure POSTNATAL4. Pourcentage de laboratoires selon le nombre de diagnostics de génétique moléculaire proposés en 2012

Activité de pharmacogénétique
En 2012, 44 laboratoires ont eu une activité de pharmacogénétique.
Le nombre d’analyses recueillies dans le rapport d’activité a presque doublé entre 2009 et 2010 puis de nouveau entre 2010 et 2011. Ce nombre est finalement stable entre 2011 et 2012 (tableau POSTNATAL12). Ce phénomène est probablement lié à deux causes. Tout d’abord, les années 2010-2011 ont vu une montée en charge de cette activité notamment avec l’arrivée en 2010-2011 de l’examen « Prédiction de la réponse au traitement Interféron/Ribavirine ». Ensuite, le travail effectué sur ce rapport d’activité et les meilleures modalités de recueil de l’information ont probablement amélioré la qualité des données les rendant plus exhaustives. Depuis trois ans, un travail important et continu entre l’Agence de la biomédecine, Orphanet et les professionnels a permis de mettre en place des codes Orpha pour la majorité des analyses de pharmacogénétique. Cet effort a permis de mieux recueillir les données. Néanmoins une amélioration continue reste nécessaire surtout pour ce domaine qui est en constante évolution. Les laboratoires devront notamment, lorsqu’ils étudient un gène, être en mesure d’en connaitre l’indication lorsqu’il peut y en avoir plusieurs. Les variations des données du tableau POSTNATAL13 concernant les examens de pharmacogénétique réalisés ou disponibles sont liées en partie à cette codification que doivent s’approprier les laboratoires.
Tableau POSTNATAL12. Evolution de l’activité de pharmacogénétique
|
2009 |
2010 |
2011 |
2012 |
Nombre d’examen de pharmacogénétique différents |
||||
Disponibles |
50 |
121 |
113 |
114 |
Réalisés |
46 |
74 |
51 |
86 |
Nombre d’examens réalisés |
6442 |
11564 |
21037 |
21701 |
Tableau POSTNATAL13. Examens de pharmacogénétique pour lesquels au moins 150 analyses ont été effectués en 2012
Numéro ORPHA |
Maladie |
Nombre d’examens |
Nombre de laboratoires ayant effectué un examen de niveau 1 |
Nombre de laboratoires ayant effectué un examen de niveau 2 |
Nombre de laboratoires total |
ORPHA284102 |
Réponse au polyéthylène glycol/interféron-ribavirine dans l'hépatite C |
4252 |
20 |
1 |
21 |
ORPHA241005 |
Susceptibilité au syndrome d'hypersensibilité à l'abacavir |
3371 |
3 |
2 |
5 |
ORPHA240839 |
Toxicité du 5-fluorouracile |
2832 |
5 |
2 |
7 |
ORPHA240885 |
Toxicité de l'irinotécan |
1743 |
9 |
3 |
12 |
ORPHA241043 |
Choix du dosage de tacrolimus dans la transplantation |
1502 |
6 |
4 |
10 |
ORPHA240927 |
Choix du dosage d'azathioprine dans le traitement de la maladie de Crohn, de la leucémie et dans la transplantation |
1243 |
12 |
2 |
14 |
ORPHA240855 |
Toxicité de la capécitabine |
807 |
4 |
2 |
6 |
ORPHA241019 |
Susceptibilité à la neutropénie dans le traitement par l'azathioprine |
599 |
11 |
4 |
15 |
ORPHA3315 |
Déficit en thiopurine S-methyltransferase |
478 |
3 |
1 |
4 |
ORPHA240853 |
Toxicité de l'azathioprine |
345 |
11 |
5 |
16 |
ORPHA240945 |
Résistance au tacrolimus dans la transplantation |
327 |
6 |
4 |
10 |
ORPHA240973 |
Susceptibilité aux effets indésirables graves de l'irinotécan |
253 |
9 |
2 |
11 |
ORPHA241045 |
Choix du dosage de la warfarine dans le traitement de la thrombose veineuse et de la fibrillation auriculaire |
232 |
5 |
3 |
8 |
ORPHA240955 |
Susceptibilité aux effets indésirables graves du 5-fluorouracile |
228 |
6 |
1 |
7 |
ORPHA240849 |
Toxicité des antipsychotiques |
209 |
1 |
3 |
4 |
