En 2017, 496 584 personnes ont bénéficié d’un examen génétique constitutionnelle (+10 % par rapport à 2016).
Un examen de génétique constitutionnelle postnatale consiste à analyser les caractéristiques génétiques héritées ou acquises à un stade précoce du développement prénatal.
Cette analyse a pour objet (Article R. 1131-1 du code de la santé publique) :
- Soit de poser, de confirmer ou d’infirmer le diagnostic d’une maladie à caractère génétique chez une personne ;
- Soit de rechercher les caractéristiques d’un ou plusieurs gènes susceptibles d’être à l’origine du développement d’une maladie chez une personne ou les membres de sa famille potentiellement concernés ;
- Soit d’adapter la prise en charge médicale d’une personne selon ses caractéristiques génétiques.
Les examens de génétique somatique et les examens réalisés dans le cadre du don (notamment analyses HLA dans le cadre de la greffe) sont en dehors du champ de la loi de bioéthique et donc de ce rapport annuel d’activité.
Différentes techniques permettent d’analyser ces caractéristiques génétiques. Si l’anomalie génétique est visible au niveau du chromosome, les techniques utilisées seront le plus souvent des techniques de cytogénétique (caryotype) y compris de cytogénétique moléculaire (hybridation in situ fluorescente : FISH). Si l’anomalie se situe au niveau de la molécule d’ADN, du gène, une technique de génétique moléculaire sera plutôt employée. Cette frontière autrefois franche entre cytogénétique et génétique moléculaire tend à disparaitre avec l’avènement de techniques qui permettent d’appréhender des remaniements chromosomiques au niveau moléculaire : analyse chromosomique par puce à ADN, techniques de séquençage à haut débit aussi appelées séquençage de nouvelle génération (NGS pour Next Generation Sequencing), ou encore séquençage massif en parallèle car permettant de tester plusieurs gènes dans une seule technique (panels de gènes).
Ce rapport d’activité de génétique postnatale constitue un outil important pour connaitre les pratiques et les besoins, notamment dans le cadre de suivi des SROS et du second plan maladies rares. Ce rapport, unique en Europe, créé relativement récemment, est en constante évolution pour s’adapter à l’évolution des pratiques.
Matériel et méthodes
Les données de génétique postnatale correspondent à l’activité 2017 des laboratoires. Elles ont été recueillies de manière spécifique en coopération avec Orphanet.Une modification du questionnaire de recueil des données d’activité a été réalisée en 2015, de façon à prendre en compte l’utilisation des techniques de séquençage à haut débit. Cette modification impacte les données d’activité de génétique moléculaire. La comparaison avec les années précédentes doit prendre en compte ce facteur.
Une première campagne dite qualitative au mois d’octobre a permis de recueillir le descriptif des panels de gènes (la technique de NGS permet dans une indication clinique donnée d’analyser en un seul examen une série de gènes impliqués) : indication du panel, maladies et gènes testés.
La base de données a été figée le 14 avril 2017. Les modifications apportées après cette date n’ont pas été prises en compte. Trois laboratoires n’ont pas transmis leur rapport d’activité avant le gel de la base de données, mais 99% (227/230) des laboratoires contactés ont rendu leur rapport annuel d’activité. Parmi les 227 laboratoires qui ont rendu leur rapport d’activité, deux laboratoires de génétique moléculaire n’ont pas eu d’activité au cours de l’année 2017.
Laboratoires de génétique postnatale
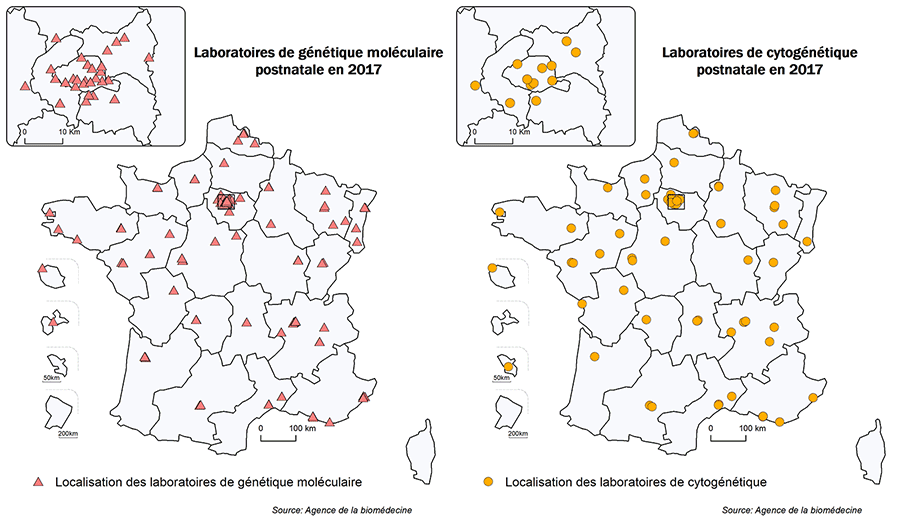
Parmi les 225 laboratoires ayant déclaré une activité à l’Agence de la biomédecine, 63 ont au moins une activité de cytogénétique y compris de cytogénétique moléculaire et 191 au moins une activité de génétique moléculaire. Vingt-neuf laboratoires réalisent les deux activités. Un peu plus d’un tiers des laboratoires autorisés pour la génétique moléculaire le sont uniquement pour une activité limitée (34,6%). Dans cette dernière situation, l’activité peut être limitée à un ou plusieurs examens de réalisation et d’interprétation généralement plus simples et qui nécessite(nt) une expertise complémentaire (exemple en hématologie, pharmacologie) (tableaux POSTNATAL1 et POSTNATAL2).Les deux cartes de la figure POSTNATAL1 montrent la répartition géographique des laboratoires sur le territoire français. Toutes les régions (hormis la Corse, la Guadeloupe, la Guyane, Mayotte non représentée) possèdent au moins un laboratoire de cytogénétique constitutionnelle. La répartition de cette activité sur le territoire donne une indication sur l’organisation et l’offre de soins nationale mais ne permet pas d'appréhender l'offre de soins de proximité. En effet, souvent les laboratoires travaillent en réseau. Les prélèvements voyageant, certains laboratoires proposent un diagnostic d’expertise pour l'ensemble de la France. Dans le contexte de l’utilisation à titre diagnostique de l’outil NGS, les laboratoires ayant une activité non limitée s’inscrivent dans les recommandations professionnelles spécifiant l’importance d’utiliser le réseau des laboratoires d’expertise de la pathologie/gène donné pour l’analyse et l’interprétation des résultats. Seule une cartographie des consultations de génétique pourrait montrer l'accès aux soins au niveau régional.
Tableau POSTNATAL1. Laboratoires ayant déclaré une activité de génétique postnatale entre 2013 et 2017
*Certains laboratoires proposent une activité de génétique moléculaire et de cytogénétique.
Tableau POSTNATAL2. Activités pratiquées par les laboratoires de génétique moléculaire ayant une autorisation limitée entre 2013 et 2017
Répartition des laboratoires de cytogénétique et de génétique moléculaire postnatale ayant déclaré une activité de génétique postnatale sur le territoire français
Figure POSTNATAL1. Répartition géographique des laboratoires de cytogénétique et de génétique moléculaire postnatale ayant déclaré une activité en 2017
Résumé de l'activité de génétique postnatale
Tableau POSTNATAL3. Résumé de l'activité de génétique postnatale entre 2013 et 2017
* Maladies répertoriées dans la classification Orphanet.
** Le nombre d'examens réalisés depuis 2015 n'est pas comparable aux années précédentes : le recueil d'information a été modifié de façon à prendre en compte l'utilisation des techniques de séquençage à haut débit.
Activité de cytogénétique
L’activité de cytogénétique postnatale qui diminuait régulièrement depuis 2014 est en croissance en 2017 avec près de 67 800 individus qui ont bénéficié d’une FISH ou d’un caryotype (tableau POSTNATAL3), soit un niveau équivalent à 2015. Cette augmentation d’activité est exclusivement liée à deux indications : « Troubles de la reproduction » et « don de gamètes ».
Avec 64 255 examens en 2017, le caryotype reste très pratiqué en génétique postnatale (tableau POSTNATAL3). Les analyses d’hybridations in situ (FISH) sont souvent réalisées en complément d’un caryotype. Les FISH réalisées dans le cadre de validation de résultats de puces ne sont pas comptabilisées ici.
Les grands groupes d’indications sont présentés dans les tableaux POSTNATAL4 et POSTNATAL5 et la figure POSTNATAL2. Depuis 2016, les indications « don de gamètes » et « recherche d'une anomalie constitutionnelle suite à la réalisation d'un examen somatique » ont été ajoutées au tableau. Auparavant comptabilisées dans « autre », elles ont été individualisées du fait de leur fréquence.
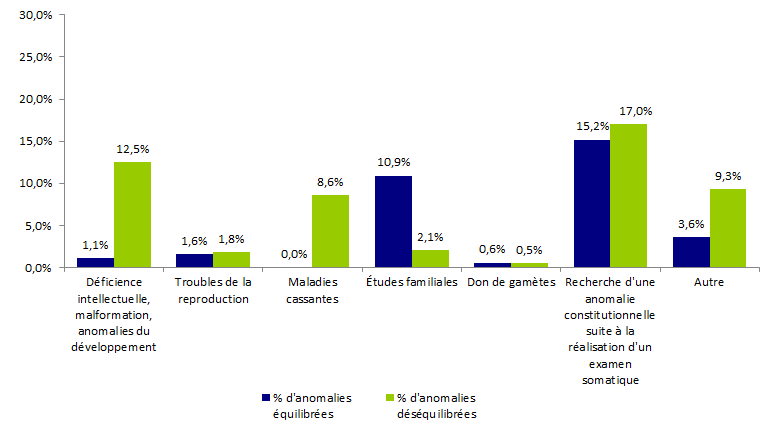
Les examens de cytogénétique postnatale les plus souvent prescrits portent sur l’indication « troubles de la reproduction » (43 854 caryotypes et 6 158 FISH). Le nombre de caryotype pour cette indication augmente de 7,6% entre 2016 et 2017. Il est à noter que le taux d’anomalies diagnostiquées équilibrées (1,6%) ou déséquilibrées (1,8%) reste particulièrement faible pour cette indication vis-à-vis des autres. L’indication « don de gamètes » a un taux encore plus faible, ce qui est attendu car il ne s’agit pas ici de patients mais de donneurs potentiels dont le profil se rapproche de celui de la population générale.
Concernant l’indication « Déficience intellectuelle, malformation, anomalies du développement », le nombre d’examen de cytogénétique chute régulièrement depuis plusieurs années : -6,8% depuis 2016 et -31,9% depuis 2013. L’explication est probablement l’utilisation pour cette indication d’autres outils de génétique : les puces à ADN (cf. chapitre puce) et les panels de gènes par NGS (cf. chapitre génétique moléculaire). Pour cette indication le pourcentage d’anomalies déséquilibrées est de 12,5%.
Pour l’indication « études familiales » le nombre de caryotypes diminue aussi (-23,8% depuis 2013 et -6,9% depuis 2016). Le taux d’anomalie équilibré diagnostiqué est important, ce qui est attendu.
Sur l’indication « recherche d'une anomalie constitutionnelle suite à la réalisation d'un examen somatique » 17,0% d’anomalies déséquilibrées sont diagnostiquées en génétique constitutionnelle par caryotype. Ce taux, le plus important, est cohérent puisqu’il s’agit d’un examen de 2nde intention après une découverte que l’on peut qualifier d’incidente lors de l’examen de la tumeur.
Tableau POSTNATAL4. Activité de cytogénétique postnatale en 2017
Tableau POSTNATAL5. Evolution de l'activité de cytogénétique postnatale selon l'indication du prélèvement entre 2013 et 2017
* Depuis 2016, les indications « don de gamètes » et « recherche d'une anomalie constitutionnelle suite à la réalisation d'un examen somatique » ont été ajoutées. Auparavant, elles étaient comptabilisées dans la catégorie « autre ».
Figure POSTNATAL2. Fréquence des anomalies identifiées par caryotype selon l'indication et le type d'anomalie en 2017
Suivi du dispositif de dépistage prénatal de la trisomie 21
En plus de ces grands groupes d’indications définis en collaboration avec les sociétés savantes de cytogénétique, l’Agence de la biomédecine recueille spécifiquement le nombre de cas de trisomies 21 diagnostiquées en génétique postnatale lorsque qu’il n’y a pas eu de diagnostic en prénatal (tableaux POSTNATAL6, POSTNATAL7 et POSTNATAL8). Cette donnée fait partie du dispositif global de suivi du dépistage de la trisomie 21 et fait l’objet d’une analyse dans ce contexte (cf. rapport annuel d’activité de diagnostic prénatal).
L’absence de diagnostic prénatal correspond à plusieurs situations : soit des femmes ayant eu un dépistage positif et ne souhaitant pas avoir de diagnostic, soit des femmes ayant eu un dépistage négatif (faux négatif), soit des femmes n’ayant eu ni dépistage par marqueurs sériques maternels ni diagnostic au cours de leur grossesse.
En 2017, il y a eu 500 naissances d’enfants diagnostiqués avec une trisomie 21 en postnatal alors qu’il n’y avait pas eu de diagnostic prénatal. Bien que ce chiffre soit fluctuant, aucune tendance à la hausse ou à la baisse ne semble se dégager sur la période 2013 à 2017.
Parmi ces naissances, le parcours prénatal des femmes est inconnu pour 33,0% d’entre elles, 28,4% des femmes n’avaient pas réalisé de dépistage et 39,2% avaient choisi d’avoir un dépistage.
Parmi les femmes ayant eu un dépistage mais n’ayant pas réalisé de diagnostic, 42,3 % étaient dans la zone à risque et 52,0 % d’entre elles ne l’étaient pas (le résultat du dépistage est inconnu pour 5,6% d’entre-elles).
Une attention particulière doit être portée sur le nombre important de parcours prénatal inconnus.
Les informations relatives aux résultats du dépistage d'aneuploïdies sur l'ADN fœtal circulant dans le sang maternel montrent que 8 enfants sont nés avec une trisomie 21 alors que le dépistage génétique non invasif avait donné un résultat négatif. Les conditions de prescription et de réalisation de l’examen sont inconnues : en France ou à l’étranger, sur des femmes à risque ou en première intention. L’interprétation de ce résultat est donc difficile et doit se faire dans le cadre plus large du suivi du dépistage. Une vigilance particulière sur l’utilisation de ce dispositif est mise en place par l’Agence de la biomédecine.
Tableau POSTNATAL6. Suivi du nombre de trisomies 21 diagnostiquées par caryotype postnatal* entre 2013 et 2017
|
|
2013 |
2014 |
2015 |
2016 |
2017 |
Nombre de cas de trisomies 21 diagnostiquées par caryotype postnatal chez les enfants nés vivants en France |
500 |
563 |
481 |
488 |
500 |
* Diagnostic postnatal de trisomie 21 d'enfants nés vivants en France sans diagnostic prénatal.
Tableau POSTNATAL7. Parcours prénatal des femmes enceintes ayant donné naissance à un enfant atteint de trisomie 21 diagnostiquée par caryotype postnatal* en 2017
* Diagnostic postnatal de trisomie 21 d'enfants nés vivants en France sans diagnostic prénatal.
Tableau POSTNATAL8. Résultat du dépistage prénatal des femmes enceintes ayant donné naissance à un enfant atteint de trisomie 21 diagnostiquée par caryotype postnatal* en 2017
* Diagnostic postnatal de trisomie 21 d'enfants nés vivants en France sans diagnostic prénatal.
Tableau POSTNATAL9. Résultat du dépistage d'aneuploïdies sur ADN fœtal circulant dans le sang maternel des femmes enceintes ayant donné naissance à un enfant atteint de trisomie 21 diagnostiquée par caryotype postnatal* en 2017
* Diagnostic postnatal de trisomie 21 d'enfants nés vivants en France sans diagnostic prénatal.
Activité de recherche d'une anomalie chromosomique par analyse moléculaire
Les recherches d’anomalies chromosomiques par analyse moléculaire sont des techniques effectuées à la fois par certains laboratoires de cytogénétique et par les laboratoires de génétique moléculaire.
L’organisation des différents laboratoires ou plateformes est très variable, ce qui rend compliqué le recueil de l’activité dans ce domaine puisqu’un même examen peut être pris en compte par plusieurs laboratoires. L’information qui a semblé la plus pertinente étant le nombre de patients ayant accès à un diagnostic par cette technologie, le choix a été fait d’analyser le nombre de dossiers rendus et pas le nombre d’analyses réalisées. Cette donnée correspond à un résultat diagnostique rendu au prescripteur après analyse des puces et validation de l’anomalie génétique identifiée par une autre technique (en général FISH ou qPCR (quantitative Polymerase Chain Reaction)).
Analyse par puces
Le rapport d’activité recense environ 18 000 dossiers d’analyses par puces rendus au prescripteur en 2017. L’utilisation des puces qui était en constante augmentation depuis 2013 semble se stabiliser en 2017 : + 1 % par rapport à l’année 2016.
La quasi-totalité des examens est réalisée pour des analyses pangénomiques et non pour des analyses ciblées (17 563 dossiers rendus versus 459). Les puces ciblées diminuent depuis 2013 avec – 15,9 % de dossier rendu entre 2016 et 2017 (et -40,2% si on compare à 2013) (tableau POSTNATAL10, tableau POSTNATAL11, figure POSTNATAL3).
L’évolution de l’activité par indication (tableau POSTNATAL13) montre que l’indication « Déficience intellectuelle ou trouble des apprentissages dans un cadre syndromique » reste plutôt stable alors que les « Troubles envahissants du développement / Autisme / Épilepsie » augmentent régulièrement depuis 2013. On observe pour cet examen +17,2% de dossiers rendus au prescripteur entre 2016 et 2017.
L’indication « Caractérisation d'une anomalie découverte au caryotype ou par une autre technique (MLPA, FISH…) » a un résultat positif dans 69,0% des cas. Ce taux, le plus important, est attendu puisque la puce est ici réalisée en 2nde intention pour préciser l’anomalie identifiée par une autre technique (tableau POSTNATAL12).
Pour l’indication « Déficience intellectuelle ou trouble des apprentissages dans un cadre syndromique » un diagnostic peut être posé dans 20,7% des cas. Le taux est de 12,0% pour les « troubles envahissants du développement / Autisme / Épilepsie ».
Figure POSTNATAL3. Evolution du nombre de dossiers d'analyses par puces rendus entre 2013 et 2017
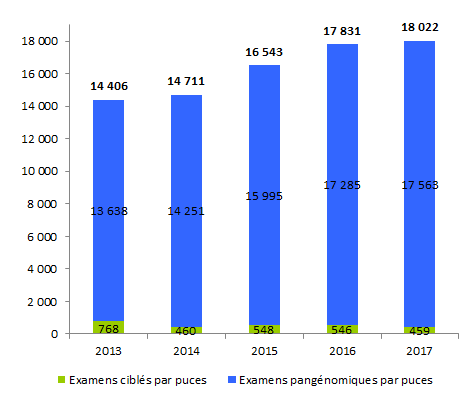
Tableau POSTNATAL10. Evolution des examens ciblés par puces entre 2013 et 2017
* Un dossier est considéré comme positif lorsqu'un résultat d'anomalie est rendu.
Tableau POSTNATAL11. Evolution de l'activité des examens pangénomiques par puces entre 2013 et 2017
* Un dossier est considéré comme positif lorsqu'un résultat d'anomalie est rendu.
Tableau POSTNATAL12. Examens pangénomiques par puces selon l'indication réalisés en 2017
Tableau POSTNATAL13. Evolution du nombre d'examens pangénomiques par puces selon l'indication entre 2013 et 2017
* Depuis 2016, l'indication « études familiales » a été ajoutée. Auparavant, elle était comptabilisée dans la catégorie « autre ».
Autres recherches d'anomalies chromosomiques par analyse moléculaire (MLPA, QF-PCR, QMPSF, etc.)
D’autres techniques de génétique moléculaire permettent la recherche d’anomalies chromosomiques, notamment : la MLPA (Multiplex ligation-dependent probe amplification), QF-PCR (Quantitative Fluorescence - polymerase chain reaction) et la QMPSF (Quantitative Multiplex PCR of Short Fragments). Une part de ces examens est réalisée dans le contexte de validation d’un autre examen, notamment d’une puce. Pour les autres situations, elles permettent le plus souvent de poser le diagnostic de maladies qui sont décrites dans la partie relative à la génétique moléculaire. Le nombre de ce type d’examens tend à diminuer depuis 2015 (tableau POSTNATAL14).
Tableau POSTNATAL14. Evolution des autres recherches d'anomalies chromosomiques par analyse moléculaire (MLPA, QF-PCR, QMPSF …) entre 2013 à 2017
Autres recherches d'anomalies chromosomiques par analyse moléculaire (MLPA, QF-PCR, QMPS, autres) |
2013 |
2014 |
2015 |
2016 |
2017 |
14 934 |
15 108 |
14 160 |
11 749 |
11 894 |
Activité de génétique moléculaire
En 2017, près de 443 500 examens de génétique moléculaire ont été réalisés en France (tableau POSTNATAL3). Ils incluaient près de 26 500 examens de pharmacogénétique (6,0%) (tableau POSTNATAL22). Au final un peu plus de 410 800 personnes ont bénéficié d’un examen de génétique moléculaire (plusieurs examens peuvent être réalisés pour une même personne).
L’identification des maladies est réalisée d’après la classification de l’encyclopédie Orphanet. Le numéro Orpha est un identifiant unique, stable dans le temps, associé à chaque entité de la classification Orphanet des maladies rares. Ces entités peuvent être des groupes de maladies, des maladies ou des sous-types de maladies. Les numéros Orpha sont destinés, entre autres, à être inclus dans les systèmes d'information en santé afin de permettre l'identification des patients ayant une maladie rare, qu'elle soit génétique ou pas.
Le numéro Orpha désigne des entités cliniques qui peuvent être associées à un ou plusieurs gènes. Ainsi peuvent être comptabilisées comme deux pathologies distinctes deux formes d’une même maladie enregistrées sous deux numéros ORPHA différents.
Chaque numéro Orpha peut correspondre à un ou plusieurs numéros OMIM également utilisés par les laboratoires.
La génétique moléculaire est en train de vivre une révolution technologique avec l’utilisation des séquenceurs de nouvelles générations (NGS).
En pratique, pour de très nombreuses maladies pouvant impliquer plusieurs gènes ou pour les pathologies qui partageaient une « porte d’entrée » clinique identique, les laboratoires testaient les gènes les uns après les autres avant l’arrivée de cette technologie.
Avec le séquençage massif parallèle (technologie NGS) les laboratoires ont pu développer des panels. Un panel est un ensemble de gènes testés pour une indication. Ainsi, lorsqu’un prélèvement nécessite plusieurs examens différents afin de poser un diagnostic il devient possible de les réaliser en une seule analyse.
L’Agence de la biomédecine a dû profondément remanier le rapport annuel d’activité en 2015 puis en 2016 pour appréhender au mieux cette évolution des pratiques. En pratique, pour un individu, avant le NGS, le nombre d’examens comptabilisés correspondait à la somme des gènes testés. Avec les panels, le nombre d’examens comptabilisés est égal à un par patient quel que soit le nombre de gènes inclus dans le panel. Dans la suite du rapport seront distinguées d’une part, les activités en lien avec le diagnostic de maladies et d’autre part, les activités en lien avec la pharmacogénétique.
Activité de génétique moléculaire appliquée aux maladies
En 2017 près 388 300 personnes ont eu un examen de génétique moléculaire, qu’il s’agisse de cas index (personne symptomatique chez qui on fait le diagnostic) ou d’apparentés (tableau POSTNATAL3 et tableau POSTNATAL22). Les laboratoires français ont réalisé des examens diagnostiques pour 3 133 maladies différentes (selon la classification Orphanet) (tableau POSTNATAL16). Ce chiffre comparable à celui de 2016 a doublé par rapport à 2015. L’explication réside dans le développement des examens utilisant les nouvelles technologies et l’évolution du rapport annuel d’activité en 2015 afin de bien prendre en compte les panels de gènes.
Parmi les laboratoires,124 déclarent travailler en lien avec une filière de santé maladies rares. Le tableau POSTNATAL15 indique le nombre de laboratoires qui appartiennent aux différentes filières de santé maladies rares. Un même laboratoire peut travailler avec plusieurs filières. On remarque une hétérogénéité importante entre les filières.
Il faut regarder avec précaution la donnée relative au nombre d’examens qui peut être surestimée lorsqu’on l’analyse par maladie (tableau POSTNATAL17) car dans les situations de panel, plusieurs maladies sont testées en même temps, la liste des maladies n’est donc pas exclusive.
Deux indications, « hémochromatose type 1 » et « thrombophilie non rare » représentent à elles seules près de 40,9% des examens réalisés en 2017 (tableau POSTNATAL18). Ces examens sont respectivement proposés par 73 et 53 laboratoires (tableau POSTNATAL17). Il s’agit des 2 seuls examens de génétique moléculaire répertoriés dans la nomenclature des actes de biologie médicale. Si en volume, ces deux tests sont importants, leur réalisation est peu couteuse et peu chronophage (variations génétiques ciblées) par rapport à l’analyse plus complexe et exhaustive de la séquence des autres gènes. Le nombre de laboratoires qui proposent ce dernier type examen augmente régulièrement.
La liste des 50 examens les plus réalisés en France (tableau POSTNATAL18) montre la présence de plusieurs maladies pour lesquelles les gènes impliqués sont des gènes de susceptibilité. Une réflexion globale sur l’intérêt de tels examens devra être menée. A titre d’exemple 72 224 (17,3%) examens ont porté sur des gènes du HLA en 2017 (hors indication de greffe et pharmacogénétique). Ce chiffre est en augmentation par rapport à 2016 (données non présentées).
Il est important de rappeler ici l’arrêté du 27 mai 2013 définissant les règles de bonnes pratiques applicables à l’examen des caractéristiques génétiques d’une personne à des fins médicales qui précise que « Les examens de génétique ne doivent être prescrits que lorsqu’ils ont une utilité clinique et qu’ils sont souhaités par la personne. Le seul fait qu’un examen soit disponible et réalisable ne justifie ni de sa prescription ni de sa réalisation » et que « de nombreux variants génétiques (polymorphismes) sont actuellement identifiés comme ne contribuant à modifier que faiblement un risque de maladie. Le risque de développer la maladie est bien inférieur à celui de la prédisposition. L’anomalie génétique n’est ni nécessaire ni suffisante pour développer la maladie ».
Les laboratoires français réalisent entre 1 et plus de 100 diagnostics de maladies différentes. Néanmoins, 22,3 % des laboratoires ne proposent qu’un ou deux diagnostics de maladies différentes (tableau POSTNATAL21). Certains laboratoires ont réalisé des analyses d’exomes : ils étaient 13 en 2017 (versus 8 en 2015). L’exome est l’analyse de l’ensemble (ou presque) des exons de tous (ou presque) les gènes d’un individu. Un exon est un segment du gène retrouvé dans l’ARN messager de ce gène (données non présentées).
Alors qu’en 2013 seuls 55 laboratoires avaient réalisé des examens en utilisant des appareils permettant des analyses NGS ils ont été 94 à le faire en 2017. Cette augmentation montre la montée en puissance de cette technologie. En 2017, environ 65 736 examens de NGS ont été rendus aux prescripteurs soit 15,8% de l’ensemble des examens de génétique moléculaire (hors pharmacogénétique) (vs. 9,3% en 2015). Cette évolution des pratiques nécessite que l’on s’assure du maintien de l’exercice en réseau des laboratoires qui individuellement ne pourront développer l’expertise nécessaire à l’interprétation des résultats obtenus sur l’ensemble d’un génome.
Les maladies génétiques sont très majoritairement rares, voire très rares. Développer des examens diagnostiques pour ces dernières peut se révéler très complexe. Ainsi, les laboratoires se sont généralement spécialisés : 89 laboratoires sont seuls à proposer le diagnostic d’une maladie pour toute la France. Au final, 983 maladies (31,4 %) ne sont diagnostiquées que dans un seul laboratoire (tableau POSTNATAL19).
La figure POSTNATAL4 montre la répartition des indications par nombre d’examens pratiqués et illustre notamment la rareté de la majorité des maladies génétiques. En effet, près de 13% des maladies ne sont recherchées au maximum que 50 fois dans l’année en France.
Le nombre d’examens est plus élevé que le nombre d’individus testés car pour une même maladie l’analyse de plusieurs gènes en parallèle ou successivement peut être nécessaire pour poser un diagnostic.
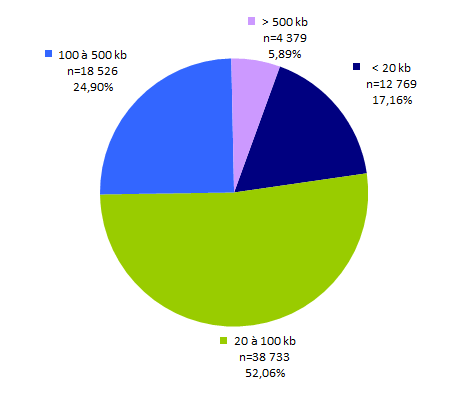
La figure POSTNATAL5 décrit la répartition des examens en fonction de la taille totale (exprimée en kb) des segments génomiques analysés. L’intérêt de cette donnée consiste principalement au suivi de la taille des panels. C’est par ailleurs l’unité de mesure choisie pour les examens réalisés par NGS dans le RIHN (Référentiel des actes Innovants Hors Nomenclature). Un quart des panels sont entre 100 et 500kb/ et près de 6% plus de 500kb. Avec la mise en place des plateformes de séquençage génomique cette donnée sera intéressante à suivre.
Par ailleurs, 604 prélèvements ont été envoyés à l’étranger par des laboratoires autorisés pour les examens des caractéristiques génétiques. Les maladies génétiques pouvant être extrêmement rares, certains examens ne sont pas proposés en France afin de garantir l’expertise d’interprétation. Au regard, du nombre d’examen total réalisés en France, la part envoyée à l’étranger reste exceptionnelle (0,15%).
Tableau POSTNATAL15. Répartitions du nombre de laboratoires selon leur appartenance aux filières de maladies rares depuis 2015
Filières de maladies rares |
Nombre de laboratoires appartenant à la filière |
||||
2015 |
2016 |
2017 |
|||
|
59 |
57 |
63 |
||
|
34 |
32 |
38 |
||
|
30 |
32 |
40 |
||
|
28 |
26 |
32 |
||
|
27 |
27 |
32 |
||
|
29 |
27 |
29 |
||
|
19 |
18 |
21 |
||
|
15 |
19 |
24 |
||
|
13 |
14 |
20 |
||
|
13 |
15 |
16 |
||
|
10 |
12 |
20 |
||
|
13 |
13 |
16 |
||
|
12 |
13 |
14 |
||
|
10 |
10 |
18 |
||
|
9 |
11 |
14 |
||
|
5 |
12 |
12 |
||
|
7 |
7 |
9 |
||
|
5 |
6 |
6 |
||
|
3 |
4 |
7 |
||
|
3 |
3 |
4 |
||
|
3 |
1 |
5 |
||
|
1 |
2 |
2 |
||
|
0 |
0 |
4 |
||
Tableau POSTNATAL16. Activité de génétique moléculaire postnatale (hors pharmacogénétique) entre 2013 et 2017
Activité de génétique moléculaire |
2013 |
2014 |
2015 |
2016 |
2017 |
Nombre de maladies différentes recherchées* |
1 252 |
1 333 |
1 490 |
3 029 |
3 133 |
Nombre d'examens rendus au prescripteur** |
404 849 |
461 936 |
385 813 |
415 211 |
416 980 |
* Maladies répertoriées dans la classification Orphanet.
** Le nombre d'examens depuis 2015 n'est pas comparable aux années précédentes : le questionnaire de recueil de données a été modifié de façon à prendre en compte l'utilisation des techniques de séquençage à haut débit.
Tableau POSTNATAL17. Nombre d'examens et de laboratoires pour les maladies recherchées par au moins quinze laboratoires par génétique moléculaire postnatale en 2017
n° ORPHA |
Maladies |
Nombre d’examens |
Nombre de laboratoires |
|
tout type de test |
panel |
|||
ORPHA64738 |
Thrombophilie non rare |
125 304 |
73 |
0 |
ORPHA139498 |
Hémochromatose type 1 |
45 298 |
53 |
6 |
ORPHA586 |
Mucoviscidose |
11 707 |
33 |
2 |
ORPHA908 |
Syndrome de l'X fragile |
14 924 |
30 |
5 |
ORPHA1646 |
Délétion partielle du chromosome Y |
4 236 |
26 |
1 |
ORPHA825 |
Spondylarthrite ankylosante |
51 304 |
25 |
0 |
ORPHA48 |
Absence congénitale bilatérale des canaux déférents |
2 978 |
22 |
1 |
ORPHA778 |
Syndrome de Rett |
4 536 |
21 |
13 |
ORPHA144 |
Syndrome de Lynch |
9 567 |
21 |
18 |
ORPHA555 |
Maladie coeliaque |
4 199 |
21 |
1 |
ORPHA117 |
Maladie de Behçet |
11 682 |
20 |
1 |
ORPHA3095 |
Syndrome de Rett atypique |
4 351 |
19 |
14 |
ORPHA145 |
Syndrome héréditaire de prédisposition au cancer du sein et de l'ovaire |
24 410 |
18 |
15 |
ORPHA243377 |
Diabète de type 1 |
1 191 |
17 |
0 |
ORPHA273 |
Dystrophie myotonique de type 1 |
2 304 |
17 |
0 |
ORPHA2073 |
Narcolepsie-cataplexie |
9 527 |
17 |
0 |
ORPHA179 |
Choriorétinopathie type birdshot |
820 |
16 |
0 |
ORPHA777 |
Déficience intellectuelle non syndromique liée à l'X |
3 344 |
16 |
13 |
ORPHA33069 |
Syndrome de Dravet |
3 810 |
16 |
14 |
ORPHA1934 |
Encéphalopathie épileptique infantile précoce |
4 454 |
16 |
15 |
ORPHA619 |
Insuffisance ovarienne précoce |
5 926 |
15 |
2 |
ORPHA109 |
Syndrome de Bannayan-Riley-Ruvalcaba |
7 088 |
15 |
15 |
ORPHA3451 |
Syndrome de West |
4 692 |
15 |
14 |
ORPHA70595 |
Syndrome d'ataxie neuropathique sensorielle-dysarthrie-ophtalmoplégie |
3 017 |
15 |
14 |
ORPHA59 |
Syndrome d'Allan-Herndon-Dudley |
3 783 |
15 |
14 |
ORPHA676 |
Pancréatite chronique héréditaire |
1 507 |
15 |
4 |
Tableau POSTNATAL18. Classement des 50 maladies faisant l'objet du plus grand nombre d'examens en 2017
Le tableau complet décrivant le nombre d'examens par indication est disponible sur le site de l'Agence de la biomédecine
n° ORPHA |
Maladies |
2015 |
2016 |
2017 |
ORPHA64738 |
Thrombophilie non rare |
92 561 |
122 361 |
125 304 |
ORPHA139498 |
Hémochromatose type 1 |
41 794 |
43 596 |
45 298 |
ORPHA825 |
Spondylarthrite ankylosante |
52 449 |
54 638 |
51 304 |
ORPHA145 et ORPHA213524 |
Syndrome héréditaire de prédisposition au cancer de l’ovaire isolé ou de l’ovaire et du sein |
20 774 |
29 234 |
33 655 |
ORPHA908 |
Syndrome de l'X fragile |
11 705 |
14 342 |
14 924 |
ORPHA586 |
Mucoviscidose |
10 490 |
10 940 |
11 707 |
ORPHA117 |
Maladie de Behçet |
7 011 |
3 465 |
11 682 |
ORPHA227535 |
Cancer du sein héréditaire |
|
2 376 |
11 465 |
ORPHA144 |
Syndrome de Lynch |
3 480 |
5 560 |
9 567 |
ORPHA2073 |
Narcolepsie-cataplexie |
2 446 |
10 222 |
9 527 |
ORPHA98715 |
Uvéite |
89 |
1 102 |
8 380 |
ORPHA109 |
Syndrome de Bannayan-Riley-Ruvalcaba |
|
3 046 |
7 088 |
ORPHA93256 |
Syndrome tremblement-ataxie lié à une prémutation de l'X fragile |
4 295 |
6 327 |
6 781 |
ORPHA201 |
Syndrome de Cowden |
238 |
2 247 |
6 682 |
ORPHA587 |
Syndrome de Muir-Torre |
|
2 177 |
6 641 |
ORPHA247798 |
Polypose adénomateuse familiale atténuée liée à MUTYH |
513 |
2 633 |
6 422 |
ORPHA619 |
Insuffisance ovarienne précoce |
5 061 |
6 527 |
5 926 |
ORPHA2869 |
Syndrome de Peutz-Jeghers |
306 |
1 823 |
5 876 |
ORPHA79076 |
Polypose juvénile infantile |
|
1 785 |
5 518 |
ORPHA247806 |
Polypose adénomateuse familiale atténuée liée à APC |
279 |
2 192 |
5 235 |
ORPHA99818 |
Syndrome de Turcot avec polypose |
196 |
1 984 |
5 217 |
ORPHA892 |
Maladie de von Hippel-Lindau |
585 |
2 665 |
5 086 |
ORPHA454840 |
Polypose adénomateuse familiale attenuée associée à NTHL1 |
|
488 |
4 992 |
ORPHA26106 |
Cancer gastrique diffus héréditaire |
690 |
741 |
4 782 |
ORPHA3451 |
Syndrome de West |
134 |
3 507 |
4 692 |
ORPHA217377 |
Syndrome de microduplication Xp11.22-p11.23 (Trisomie Xp11.22-p11.23) |
|
2 446 |
4 582 |
ORPHA29072 |
Phéochromocytome-paragangliome héréditaire |
2 577 |
2 769 |
4 566 |
ORPHA778 |
Syndrome de Rett |
874 |
3 263 |
4 536 |
ORPHA100 |
Ataxie-télangiectasie |
56 |
775 |
4 480 |
ORPHA1934 |
Encéphalopathie épileptique infantile précoce |
1 050 |
3 331 |
4 454 |
ORPHA3095 |
Syndrome de Rett atypique |
746 |
3 316 |
4 351 |
ORPHA155 |
Cardiomyopathie hypertrophique familiale isolée |
3 033 |
2 639 |
4 329 |
ORPHA1646 |
Délétion partielle du chromosome Y |
3 787 |
4 536 |
4 236 |
ORPHA447877 |
Polypose adénomateuse associée aux ADN polymérases |
|
1 172 |
4 219 |
ORPHA79665 |
Syndrome de Gardner |
196 |
1 984 |
4 203 |
ORPHA555 |
Maladie cœliaque |
2 015 |
3 759 |
4 199 |
ORPHA99361 |
Cancer médullaire de la thyroïde familial |
23 |
2 069 |
4 079 |
ORPHA157794 |
Polypose mixte héréditaire |
|
1 785 |
4 068 |
ORPHA329971 |
Polypose juvénile généralisée/Polypose juvénile colorectale |
|
1 785 |
4 068 |
ORPHA652 |
Néoplasie endocrinienne multiple type 1 |
1 138 |
1 639 |
3 926 |
ORPHA247709 |
Néoplasie endocrinienne multiple type 2B |
|
2 069 |
3 880 |
ORPHA209370 |
Encéphalopathie néonatale sévère avec microcéphalie |
|
2 786 |
3 879 |
ORPHA306 |
Epilepsie infantile familiale bénigne |
19 |
2 773 |
3 869 |
ORPHA33069 |
Syndrome de Dravet |
887 |
3 119 |
3 810 |
ORPHA31709 |
Syndrome de convulsions infantiles-choréoathétose |
16 |
2 607 |
3 800 |
ORPHA59 |
Syndrome d'Allan-Herndon-Dudley |
54 |
2 770 |
3 783 |
ORPHA247698 |
Néoplasie endocrinienne multiple type 2A |
33 |
2 069 |
3 778 |
ORPHA199343 |
Syndrome EAST |
|
2 824 |
3 756 |
ORPHA178469 |
Déficience intellectuelle non syndromique autosomique dominante |
179 |
2 884 |
3 683 |
Tableau POSTNATAL18b. Compléments
Figure POSTNATAL4. Répartition des maladies par nombre d'examens réalisés en 2017
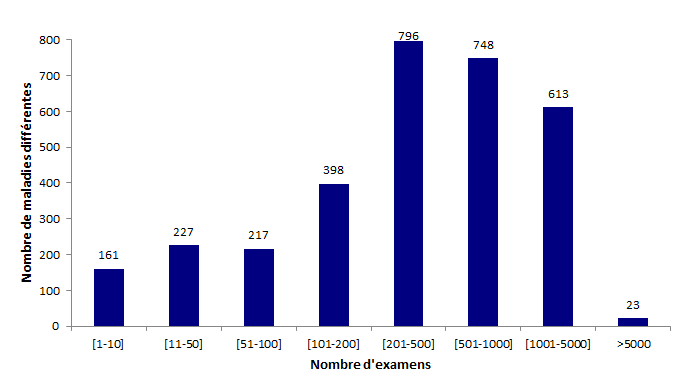
Tableau POSTNATAL19. Description de l'activité de génétique moléculaire postnatale entre 2013 et 2017
|
2013 |
2014 |
2015 |
2016 |
2017 |
Nombre de laboratoires |
|
|
|
|
|
qui n'étudient que l'hémochromatose type 1 et la thrombophilie non rare |
11 |
8 |
8 |
10 |
9 |
qui n'étudient que la thrombophilie non rare |
18 |
20 |
23 |
21 |
21 |
Nombre de laboratoires |
|
|
|
|
|
qui diagnostiquent une maladie qui n'est étudiée que dans 1 laboratoire en France |
95 |
99 |
91 |
86 |
89 |
qui diagnostiquent une maladie qui n'est étudiée que dans 2 laboratoires en France |
96 |
97 |
97 |
93 |
98 |
Nombre de maladies |
|
|
|
|
|
qui ne sont étudiées que dans 1 laboratoire en France |
803 |
840 |
956 |
976 |
983 |
qui ne sont étudiées que dans 2 laboratoires en France |
246 |
282 |
298 |
614 |
658 |
Tableau POSTNATAL20. Evolution de l'activité de diagnostic suite à un dépistage néonatal de la mucoviscidose entre 2013 et 2017
|
2013 |
2014 |
2015 |
2016 |
2017 |
Nombre de laboratoires ayant eu une activité de diagnostic suite à un dépistage néonatal de la mucoviscidose |
8 |
10 |
8 |
8 |
7 |
Nombre de nouveaux nés analysés |
3 145 |
2 890 |
2 589 |
3 260 |
3 964 |
Nombre de cas positifs rendus (2 mutations) |
73 |
137 |
109 |
80 |
80 |
Tableau POSTNATAL21. Evolution du pourcentage de laboratoires selon le nombre de diagnostics de génétique moléculaire proposés entre 2013 et 2017
Nombre de diagnostics de génétique moléculaire proposés* |
Laboratoires |
|||||||||
2013 |
2014 |
2015** |
2016 |
2017 |
||||||
N |
% |
N |
% |
N |
% |
N |
% |
N |
% |
|
1 à 2 |
53 |
29,6 |
46 |
26,3 |
46 |
26,1 |
46 |
25,6 |
41 |
22,3 |
3 à 10 |
58 |
32,4 |
59 |
33,7 |
59 |
33,5 |
50 |
27,8 |
55 |
29,9 |
11 à 20 |
26 |
14,5 |
27 |
15,4 |
20 |
11,4 |
15 |
8,3 |
13 |
7,1 |
21 à 35 |
22 |
12,3 |
22 |
12,6 |
20 |
11,4 |
17 |
9,4 |
14 |
7,6 |
36 à 100 |
19 |
10,6 |
19 |
10,9 |
27 |
15,3 |
23 |
12,8 |
28 |
15,2 |
> 100 |
1 |
0,6 |
2 |
1,1 |
4 |
2,3 |
29 |
16,1 |
33 |
17,9 |
Total |
179 |
100,0 |
175 |
100,0 |
176 |
100,0 |
180 |
100,0 |
184 |
100,0 |
* Diagnostics répertoriés dans la classification Orphanet.
** En 2015, 178 laboratoires ont eu une activité de génétique moléculaire, 2 d'entre eux n'ont pas renseigné les diagnostics proposés dans leur laboratoire.
Figure POSTNATAL5. Evolution de la répartition des examens (avec utilisation des panels) en fonction de la quantité d'acide nucléique analysée en kilobases (Kb) en 2017
Activité de génétique moléculaire appliquée à la pharmacogénétique
La pharmacogénétique est l’étude du lien entre certaines caractéristiques génétiques constitutionnelles d’un individu et la réponse de l’organisme à un ou plusieurs médicaments. La prescription des tests de pharmacogénétique dépend donc étroitement de la prescription de certains médicaments et de l’évolution des traitements. En 2017, 22 235 individus ont bénéficié d’un examen de pharmacogénétique. Ce nombre augmente régulièrement depuis 2015. Cinquante-quatre laboratoires ont déclaré avoir réalisé ces examens. (tableau POSTNATAL22)
Le nombre d’examens de pharmacogénétique réalisés a augmenté de 12,0%. (tableau POSTNATAL22). Il faut néanmoins regarder avec précaution la donnée relative au nombre d’examens qui peut être surestimée lorsqu’on l’analyse par indication (tableau POSTNATAL24) car dans les situations de panel il n’a pas été possible de distinguer les différentes indications ce qui engendre des doublons.
On peut observer que la réalisation d’examens « toxicité de l’abacavir » reste l’examen le plus réalisé en 2017 avec 7 504 examens soit 28,4% de l’ensemble des examens de pharmacogénétique (tableau POSTNATAL23 et tableau POSTNATAL24).
Le nombre d’examens réalisés pour l’indication « réponse au traitement antiviral dans l'hépatite C » voit son nombre d’examens chuter de près de 99% entre 2013 et 2017. Cette diminution (il n’a été réalisé en 2017 que 51 fois) est directement en relation avec la diminution de la prescription du médicament lié à cet examen de pharmacogénétique. Il devrait disparaitre complètement avec l’apparition des nouveaux traitements de l’hépatite C
Un nouvel examen réalisé par un seul laboratoire : « Gaucher mise sous Eliglustat » a été proposé pour la première fois en 2016. Cet examen est exigé avant prescription dans les RCP (résumé des caractéristiques du produit) du médicament.
La majorité des autres médicaments associés à un examen de pharmacogénétique correspond à des anticancéreux.
Tableau POSTNATAL22. Evolution de l'activité de pharmacogénétique entre 2013 et 2017*
Activité de pharmacogénétique |
2012 |
2013 |
2014 |
2015 |
2016 |
2017 |
Nombre d'individus testés |
|
|
|
18 777 |
20 147 |
22 535 |
Nombre d'examens réalisés |
20 425 |
25 303 |
19 596 |
19 909 |
23 627 |
26 458 |
Nombre de laboratoires avec activité de pharmacogénétique |
44 |
47 |
53 |
47 |
51 |
54 |
Nombre de laboratoires ayant uniquement pratiqué une activité de pharmacogénétique |
5 |
5 |
5 |
5 |
5 |
7 |
* Une modification de la classification des indications de pharmacogénétique a été réalisée en 2014. Cette modification impacte le recueil de l'activité. Toute comparaison avec les années précédentes doit tenir compte de ce changement.
Tableau POSTNATAL23. Examens de pharmacogénétique effectués en 2017
ORPHA |
Indications de l'examen* |
Nombre de laboratoires |
Nombre d'examens |
ORPHA240841 |
Toxicité de l'abacavir |
22 |
7 504 |
ORPHA240839 |
Toxicité des dérivés du fluorouracile |
17 |
5 498 |
ORPHA413687 |
Toxicité et adaptation posologique de l'azathioprine ou 6-mercaptopurine |
21 |
3 197 |
ORPHA240947 |
Résistance au tamoxifène |
4 |
2 282 |
ORPHA241043 |
Adaptation posologique du tacrolimus |
12 |
2 201 |
ORPHA240885 |
Toxicité de l'irinotécan |
19 |
2 122 |
ORPHA240863 |
Toxicité du cisplatine |
12 |
1 557 |
ORPHA413667 |
Toxicité et adaptation posologique des antidépresseurs ou antipsychotiques |
7 |
1 449 |
ORPHA240935 |
Résistance au clopidogrel |
6 |
858 |
ORPHA240921 |
Toxicité du voriconazole |
6 |
855 |
ORPHA240867 |
Toxicité de la codéine |
3 |
378 |
AutrePharma2 |
Gaucher mis sous éliglustat |
1 |
360 |
ORPHA240905 |
Toxicité du raltegravir |
7 |
228 |
ORPHA413674 |
Toxicité et adaptation posologique des anti-vitamines K |
7 |
201 |
ORPHA413690 |
Toxicité et adaptation posologique du méthotrexate |
7 |
167 |
ORPHA413684 |
Résistance aux anti-vitamines K |
5 |
96 |
ORPHA284113 |
Susceptibilité aux effets indésirables graves de la mercaptopurine |
2 |
78 |
ORPHA284102 |
Réponse au traitement anti-viral dans l'hépatite C |
7 |
51 |
ORPHA413693 |
Toxicité des curarisants |
3 |
50 |
ORPHA284121 |
Toxicité ou non réponse au clozapine |
2 |
29 |
ORPHA240869 |
Toxicité de l'éfavirenz |
2 |
18 |
ORPHA413681 |
Surdosage ou adaptation posologique des hypoglycémiants oraux |
2 |
18 |
ORPHA240887 |
Toxicité de l'isoniazide |
3 |
15 |
ORPHA413696 |
Toxicité des statines |
4 |
10 |
* Indications répertoriées dans la classification Orphanet.
Tableau POSTNATAL24. Evolution du nombre d'examens de pharmacogénétique entre 2013 et 2017**
ORPHA |
Indication de l'examen* |
2013 |
2014 |
2015 |
2016 |
2017 |
ORPHA240841 |
Toxicité de l'abacavir |
6 417 |
6 707 |
7 464 |
8 041 |
7 504 |
ORPHA240839 |
Toxicité des dérivés du fluorouracile |
3 643 |
3 387 |
3 321 |
4 481 |
5 498 |
ORPHA413687 |
Toxicité et adaptation posologique de l'azathioprine ou 6-mercaptopurine |
3 084 |
2 091 |
2 817 |
3 325 |
3 197 |
ORPHA240947 |
Résistance au tamoxifène |
48 |
4 |
207 |
537 |
2 282 |
ORPHA241043 |
Adaptation posologique du tacrolimus |
1 351 |
1 720 |
2 063 |
1 948 |
2 201 |
ORPHA240885 |
Toxicité de l'irinotécan |
2 283 |
1 784 |
1 814 |
1 897 |
2 122 |
ORPHA240863 |
Toxicité du cisplatine |
586 |
43 |
2 042 |
1 671 |
1 557 |
ORPHA413667 |
Toxicité et adaptation posologique des antidépresseurs ou antipsychotiques |
1 373 |
614 |
871 |
1 262 |
1 449 |
ORPHA240935 |
Résistance au clopidogrel |
124 |
84 |
438 |
817 |
858 |
ORPHA240921 |
Toxicité du voriconazole |
24 |
29 |
424 |
762 |
855 |
ORPHA240867 |
Toxicité de la codéine |
48 |
1 |
138 |
142 |
378 |
AutrePharma2 |
Gaucher mis sous Eliglustat |
|
|
|
395 |
360 |
ORPHA240905 |
Toxicité du raltegravir |
336 |
1 |
240 |
244 |
228 |
ORPHA413674 |
Toxicité et adaptation posologique des anti-vitamines K |
519 |
678 |
377 |
249 |
201 |
ORPHA413690 |
Toxicité et adaptation posologique du méthotrexate |
94 |
44 |
95 |
151 |
167 |
ORPHA413684 |
Résistance aux anti-vitamine K |
115 |
37 |
216 |
173 |
96 |
ORPHA284113 |
Susceptibilité aux effets indésirables graves de la mercaptopurine |
|
|
133 |
117 |
78 |
ORPHA284102 |
Réponse au traitement anti-viral dans l'hépatite C |
4 287 |
2 215 |
898 |
288 |
51 |
ORPHA413693 |
Toxicité des curarisants |
228 |
11 |
71 |
47 |
50 |
ORPHA284121 |
Toxicité ou non réponse au clozapine |
12 |
22 |
18 |
18 |
29 |
ORPHA240869 |
Toxicité de l'efavirenz |
83 |
80 |
16 |
7 |
18 |
ORPHA413681 |
Surdosage ou adaptation posologique des hypoglycémiants oraux |
190 |
1 |
37 |
9 |
18 |
ORPHA240887 |
Toxicité de l'isoniazide |
40 |
19 |
24 |
23 |
15 |
ORPHA413696 |
Toxicité des statines |
42 |
3 |
40 |
4 |
10 |
ORPHA357194 |
Choix d'une option thérapeutique pour le cancer colorectal |
|
|
|
6 |
|
ORPHA464458 |
Intoxication au paracétamol |
|
|
4 |
|
|
* Indications répertoriées dans la classification Orphanet.
** Une modification de la classification des indications de pharmacogénétique a été réalisée en 2014. Cette modification impacte le recueil de l'activité. Toute comparaison avec les années précédentes doit tenir compte de ce changement.