En 2014 près 480 000 personnes ont bénéficié d’un examen génétique.
Un examen de génétique postnatale consiste à analyser les caractéristiques génétiques héritées ou acquises à un stade précoce du développement prénatal.
Cette analyse a pour objet (Article R. 1131-1 du code de la santé publique) :
-
Soit de poser, de confirmer ou d’infirmer le diagnostic d’une maladie à caractère génétique chez une personne;
-
Soit de rechercher les caractéristiques d’un ou plusieurs gènes susceptibles d’être à l’origine du développement d’une maladie chez une personne ou les membres de sa famille potentiellement concernés;
-
Soit d’adapter la prise en charge médicale d’une personne selon ses caractéristiques génétiques.
Les examens de génétique somatique et les examens réalisés dans le cadre du don (notamment analyses HLA dans le cadre de la greffe) sont en dehors du champ de la loi de bioéthique et donc de ce rapport annuel d’activité.
Différentes techniques permettent d’analyser ces caractéristiques génétiques. Si l’anomalie génétique est visible au niveau du chromosome, les techniques utilisées seront le plus souvent des techniques de cytogénétique (caryotype) y compris de cytogénétique moléculaire (FISH). Si l’anomalie se situe au niveau de la molécule d’ADN, du gène, une technique de génétique moléculaire sera plutôt employée. Cette frontière autrefois franche entre cytogénétique et génétique moléculaire tend à disparaitre avec l’avènement de techniques qui permettent d’appréhender des remaniements chromosomiques au niveau moléculaire (analyse chromosomique par puce à ADN ; techniques de séquençage à haut débit aussi appelées séquençage de nouvelle génération (NGS)).
Ce rapport d’activité de génétique postnatale constitue un outil important notamment dans le cadre de suivi des SROS et du second plan maladies rares. Ce rapport unique en Europe, créé relativement récemment, est en constante évolution pour s’adapter aux évolutions des pratiques.
Matériel et méthodes
Les données de génétique postnatale correspondent à l’activité 2014 des laboratoires. Elles ont été recueillies de manière spécifique en coopération avec Orphanet.
La base de données a été figée le 3 mars 2015. Les modifications apportées après cette date n’ont pas été prises en compte.
Un laboratoire de cytogénétique et un laboratoire de génétique moléculaire n’ont pas transmis leur rapport d’activité avant le gel de la base de données, cependant près de 99% (225/227) des laboratoires contactés ont rendu leur rapport annuel d’activité.
Laboratoires de génétique postnatale
Parmi les 225 laboratoires ayant déclaré une activité à l’Agence de la biomédecine, 71 ont au moins une activité de cytogénétique y compris de cytogénétique moléculaire et 180 au moins une activité de génétique moléculaire. Vingt-six laboratoires ont les deux activités. Un peu plus d’un tiers des laboratoires autorisés pour la génétique moléculaire le sont uniquement pour une activité limitée. Dans cette dernière situation, l’activité peut être limitée à un ou plusieurs examens de réalisation et d’interprétation généralement plus simples et qui nécessite une expertise complémentaire (exemple en hématologie) (Tableaux POSTNATAL1 et POSTNATAL2).
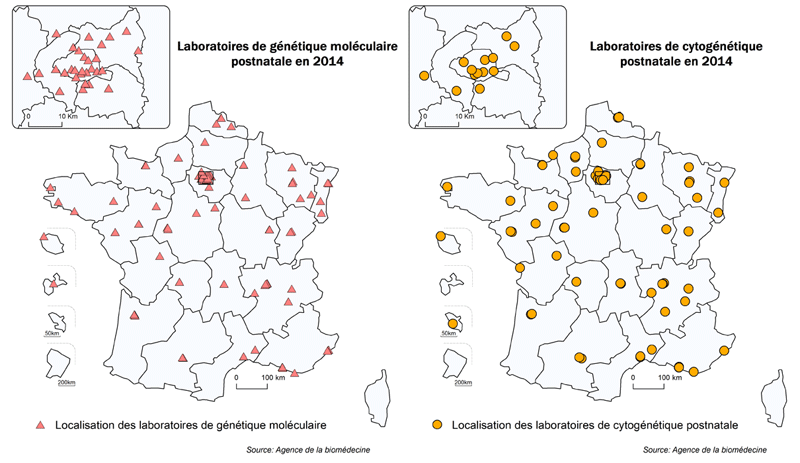
Les deux cartes de la figure POSTNATAL1 montrent la répartition géographique des laboratoires sur le territoire français. Toutes les régions (hormis la Corse, la Guadeloupe et la Guyane) possèdent au moins un laboratoire de cytogénétique constitutionnelle. La répartition de cette activité sur le territoire donne une indication sur l’organisation et l’offre de soins. En revanche, la répartition géographique de l’activité de génétique moléculaire ne donne d’information que sur l'existence des laboratoires mais en aucun cas ne permet d'appréhender l'offre de soins de proximité. Souvent les laboratoires travaillent en réseau. En effet, les prélèvements voyageant, certains d’entre eux proposent un diagnostic d’expertise pour l'ensemble de la France. Les laboratoires ayant une activité non limitée ne peuvent pas et ne doivent pas développer un catalogue complet de diagnostics car ils doivent maintenir l’expertise nécessaire à l’analyse et l’interprétation des résultats. Seule une cartographie des consultations de génétique pourrait montrer l'accès aux soins au niveau régional.
Tableau POSTNATAL1. Laboratoires ayant une activité de génétique postnatale d'après les déclarations faites dans les rapports d'activité
2010 |
2011 |
2012 |
2013 |
2014 |
|
Nombre de laboratoires avec une activité de cytogénétique |
73 |
76 |
73 |
70 |
71 |
Nombre de laboratoires avec une activité de génétique moléculaire |
177 |
180 |
180 |
184 |
180 |
. avec une activité à autorisation non limitée |
106 |
104 |
110 |
121 |
110 |
. avec une activité à autorisation limitée |
71 |
76 |
70 |
63 |
70 |
Nombre total de laboratoires* |
233 |
235 |
232 |
231 |
225 |
* Certains laboratoires proposent une activité de génétique moléculaire et de cytogénétique (soit 26 en 2014)
Tableau POSTNATAL2. Activités pratiquées par les laboratoires de génétique moléculaire ayant une autorisation limitée
Nombre de laboratoires |
|||||
2010 |
2011 |
2012 |
2013 |
2014 |
|
Facteurs II et V |
43 |
36 |
35 |
35 |
37 |
Hématologie |
22 |
20 |
18 |
16 |
18 |
Hémochromatose |
16 |
14 |
16 |
13 |
11 |
Analyses de biologie moléculaire appliquée à la cytogénétique |
10 |
3 |
3 |
2 |
4 |
Pharmacogénétique |
9 |
12 |
8 |
11 |
12 |
Typages HLA |
4 |
6 |
8 |
9 |
12 |
Autre |
28 |
29 |
24 |
18 |
14 |
Répartition des laboratoires de cytogénétique et de génétique moléculaire postnatale ayant déclaré une activité de génétique postnatale sur le territoire français
Figure POSTNATAL1. Répartition géographique des laboratoires de cytogénétique et de génétique moléculaire postnatale ayant déclaré une activité en 2014
Résumé de l'activité de génétique postnatale
Tableau POSTNATAL3. Résumé de l'activité de génétique postnatale
2010 |
2011 |
2012 |
2013 |
2014 |
|
Cytogénétique |
. |
. |
. |
. |
. |
Nombre d'individus testés |
72516 |
74334 |
72850 |
68370 |
68568 |
Nombre total d'analyses |
84933 |
85015 |
82798 |
77168 |
78229 |
. par caryotype |
71000 |
71553 |
69405 |
66049 |
66014 |
. par FISH |
13933 |
13462 |
13393 |
11119 |
12215 |
Génétique moléculaire (y compris pharmacogénétique) |
. |
. |
. |
. |
. |
Nombre d'individus testés |
274273 |
329638 |
323158 |
357841 |
397798 |
Nombre de diagnostics de maladies* différentes |
. |
. |
. |
. |
. |
. disponibles |
1119 |
1238 |
1392 |
1466 |
1554 |
. réalisés |
976 |
1041 |
1194 |
1275 |
1355 |
Nombre de gènes |
. |
. |
. |
. |
. |
. disponibles |
1231 |
1405 |
1511 |
1592 |
1765 |
. testés |
1112 |
1238 |
1340 |
1441 |
1591 |
Nombre d'examens réalisés |
361168 |
388159 |
415627 |
430152 |
481532 |
Puces |
. |
. |
. |
. |
. |
Nombre de dossiers rendus |
11285 |
10104 |
12133 |
14406 |
14711 |
*Maladies répertoriées dans la classification Orphanet
Activité de cytogénétique
L’activité de cytogénétique postnatale a diminué depuis 2010. Elle est néanmoins stable entre 2013 et 2014 avec environ 68 500 individus ayant bénéficié de FISH ou d’un caryotype (Tableau POSTNATAL3).
Il est important de noter que parmi les 2 laboratoires qui n’ont pas rendu leur rapport d’activités dans les temps, l’un est un laboratoire de cytogénétique qui en 2013 avait déclaré près de 1 000 caryotypes et une cinquantaine de FISH.
Avec 66 014 examens en 2014, le caryotype reste très pratiqué en génétique postnatale (Tableau POSTNATAL3).
Les analyses d’hybridations in situ (FISH) sont souvent réalisées en complément d’un caryotype. En revanche, les FISH réalisées dans le cadre de validation de résultats de puces ne sont pas comptabilisées ici.
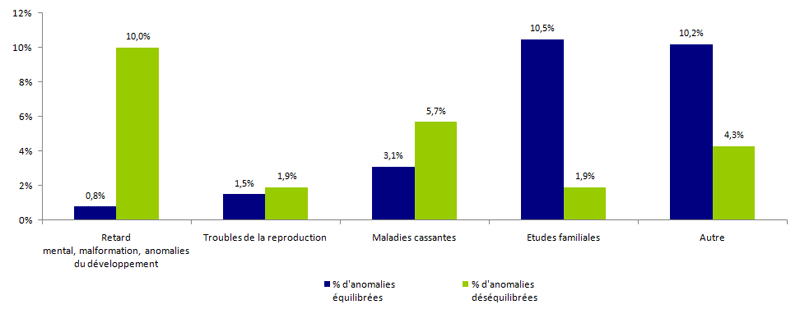
Les grands groupes d’indications sont présentés dans le tableau POSTNATAL4. Les examens de cytogénétique postnatale sont plus souvent prescrits pour expliquer un trouble de la reproduction, mais le taux d’anomalies diagnostiquées pour cette indication est le plus faible (Figure POSTNATAL2). Ce taux reste néanmoins nettement inférieur à celui observé dans la population générale.
En plus de ces grands groupes d’indications définis en collaboration avec les sociétés savantes de cytogénétique, l’Agence de la biomédecine recueille spécifiquement le nombre de cas de trisomies 21 diagnostiquées en génétique postnatale lorsque qu’il n’y a pas eu de diagnostic en prénatal (Tableau POSTNATAL6). L’absence de DPN (diagnostic prénatal) correspond à plusieurs situations : soit des femmes ayant eu un dépistage positif et ne souhaitant pas avoir de diagnostic, soit des femmes ayant eu un dépistage négatif (faux négatif) soit des femmes n’ayant pas eu ni de dépistage ni de diagnostic au cours de la grossesse. Cette donnée fait partie du dispositif global de suivi du dépistage de la trisomie 21 et fait l’objet d’une analyse dans ce contexte (cf. rapport annuel d’activité de diagnostic prénatal). En 2014, 563 diagnostics postnatals de trisomies 21 ont été posés par les laboratoires de cytogénétique. La fiabilité de cette donnée interroge. Une fluctuation de ce chiffre est observée sans que l’on puisse conclure à une hausse ou une baisse. Cette donnée devrait être consolidée avec celle du laboratoire de cytogénétique qui n’a pas adressé son rapport annuel d’activité dans les délais.
Tableau POSTNATAL4. Activité 2014 de cytogénétique postnatale
Indications |
Techniques |
Nombre |
Nombre |
Nombre |
Nombre |
Déficience intellectuelle, malformation, anomalies du développement |
Caryotype |
16096 |
14347 |
136 |
1613 |
FISH |
5809 |
4600 |
82 |
1127 |
|
Troubles de la reproduction |
Caryotype |
40422 |
39050 |
613 |
759 |
FISH |
2950 |
2005 |
413 |
532 |
|
Maladies cassantes |
Caryotype |
318 |
290 |
10 |
18 |
FISH |
3 |
2 |
0 |
1 |
|
Etudes familiales |
Caryotype |
6413 |
5622 |
672 |
119 |
FISH |
2903 |
2079 |
349 |
475 |
|
Autre |
Caryotype |
2765 |
2363 |
283 |
119 |
FISH |
550 |
293 |
135 |
122 |
|
Total |
Caryotype |
66014 |
61672 |
1714 |
2628 |
FISH |
12215 |
8979 |
979 |
2257 |
Tableau POSTNATAL5. Evolution de l'activité de cytogénétique postnatale selon l'indication du prélèvement
Nombre d'examens |
||||||
Indications |
Techniques |
2010 |
2011 |
2012 |
2013 |
2014 |
Déficience intellectuelle, malformation, anomalies du développement |
Caryotype |
19565 |
18730 |
18643 |
16415 |
16096 |
FISH |
7722 |
7735 |
7174 |
5652 |
5809 |
|
Troubles de la reproduction |
Caryotype |
40643 |
41712 |
40361 |
39652 |
40422 |
FISH |
2583 |
2125 |
2244 |
2549 |
2950 |
|
Maladies cassantes |
Caryotype |
269 |
281 |
283 |
280 |
318 |
FISH |
28 |
23 |
19 |
6 |
3 |
|
Etudes familiales |
Caryotype |
7783 |
8119 |
7716 |
7044 |
6413 |
FISH |
3188 |
3165 |
3473 |
2544 |
2903 |
|
Autre |
Caryotype |
2740 |
2711 |
2402 |
2658 |
2765 |
FISH |
412 |
414 |
483 |
368 |
550 |
|
Total |
Caryotype |
71000 |
71553 |
69405 |
66049 |
66014 |
FISH |
13933 |
13462 |
13393 |
11119 |
12215 |
|
Tableau POSTNATAL6. Suivi du nombre de trisomies 21 diagnostiquées par caryotype postnatal*
2010 |
2011 |
2012 |
2013 |
2014 |
|
Nombre de cas de trisomies 21 diagnostiquées par caryotype postnatal chez des enfants nés vivants en France |
453 |
535 |
488 |
500 |
563 |
* Diagnostic postnatal de trisomies 21 d’enfants nés vivants en France sans diagnostic prénatal
Figure POSTNATAL2. Fréquence des anomalies identifiées par caryotype en 2014 selon l'indication et le type d'anomalie
Activité de recherche d'une anomalie chromosomique par analyse moléculaire
Les recherches d’anomalies chromosomiques par analyse moléculaire sont des techniques aussi bien utilisées par les laboratoires de cytogénétique que par les laboratoires de génétique moléculaire.
L’organisation des différents laboratoires ou plateformes est très variable, ce qui rend compliqué le recueil de l’activité dans ce domaine puisqu’un même examen peut être pris en compte par plusieurs laboratoires. L’information qui a semblé la plus pertinente étant le nombre de patients ayant accès à un diagnostic par cette technologie, le choix a été fait d’analyser le nombre de dossiers rendus et pas le nombre d’analyses réalisées. Cette donnée correspond à un résultat diagnostique rendu au prescripteur après analyse des puces et validation de l’anomalie génétique identifiée par une autre technique (en général FISH ou qPCR (quantitative Polymerase Chain Reaction)).
Analyse par puces
Au total, le rapport d’activité recense un peu plus de 14 700 dossiers d’analyses par puces rendus au prescripteur en 2014. On observe une très légère augmentation de l’activité (+2,1%) entre 2013 et 2014. Cette augmentation est bien moindre qu’entre 2012 et 2013 (+18,7%). (Figure POSTNATAL3).
Dans près de 97% des cas, les puces sont utilisées pour des analyses pangénomiques et non pour des analyses ciblées. On observe une diminution du nombre de puces ciblées. Cette diminution est très probablement liée à un transfert de cette activité vers le NGS (Next Generation Sequencing).
Parallèlement le nombre de puces pangénomiques rendues aux prescripteurs est proche de celui de l’année dernière. Une augmentation plus importante de l’activité était attendue. Plusieurs facteurs peuvent expliquer ce phénomène. Comme pour les puces ciblées il est probable qu’une partie de l’activité notamment pour l’indication majoritaire « Déficience intellectuelle ou trouble des apprentissages dans un cadre syndromique» soit transférée vers la technologie du NGS. Il faudra vérifier cette hypothèse. Un autre élément à prendre en compte est le financement des puces. Elles ne sont pas à la nomenclature et leur financement initial n’avait pas prévu un tel besoin.
Figure POSTNATAL3. Evolution du nombre de dossiers d'analyses par puces rendus
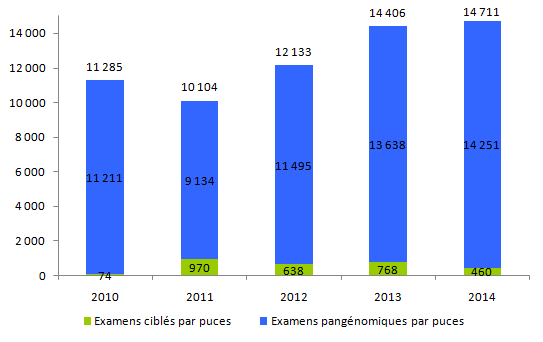
Tableau POSTNATAL7. Evolution des examens ciblés par puces
Analyses ciblées par puces |
|||||
2010 |
2011 |
2012 |
2013 |
2014 |
|
Nombre de laboratoires |
5 |
12 |
12 |
11 |
11 |
Nombre de dossiers rendus |
74 |
970 |
638 |
768 |
460 |
Nombre de dossiers positifs rendus |
32 |
375 |
234 |
145 |
72 |
% de dossiers positifs* rendus |
43,2% |
38,7% |
36,7% |
18,9% |
15,7% |
* Un dossier est considéré comme positif lorsqu’un résultat d’anomalie est rendu
Tableau POSTNATAL8. Examens pangénomiques par puces en 2014
Indications |
Nombre de |
Nombre de |
% de dossiers |
Déficience intellectuelle ou trouble des apprentissages dans un cadre syndromique |
5431 |
1317 |
24,2% |
Malformations sans retard psychomoteur |
1736 |
302 |
17,4% |
Déficience intellectuelle ou trouble des apprentissages isolés |
2301 |
442 |
19,2% |
Troubles envahissants du développement (TED)/ Autisme |
1869 |
294 |
15,7% |
Caractérisation d'une anomalie découverte au caryotype ou par une autre technique (MLPA, FISH,...) |
346 |
219 |
63,3% |
Fœtopathologie |
684 |
113 |
16,5% |
Autres |
1884 |
376 |
20,0% |
Total |
14251 |
3063 |
21,5% |
Tableau POSTNATAL9. Evolution du nombre d'examens pangénomiques par puces
Nombre de dossiers rendus |
|||||
Indications |
2010 |
2011 |
2012 |
2013 |
2014 |
Déficience intellectuelle ou trouble des apprentissages dans un cadre syndromique |
5499 |
4555 |
5339 |
5474 |
5431 |
Malformations sans retard psychomoteur |
1788 |
559 |
1117 |
1453 |
1736 |
Déficience intellectuelle ou trouble des apprentissages isolés |
661 |
1511 |
2208 |
2476 |
2301 |
Troubles envahissants du développement (TED)/ Autisme |
211 |
595 |
1108 |
1446 |
1869 |
Caractérisation d'une anomalie découverte au caryotype ou par une autre technique (MLPA, FISH,...) |
. |
661 |
346 |
481 |
346 |
Fœtopathologie |
. |
548 |
632 |
742 |
684 |
Autres |
3052 |
705 |
745 |
1566 |
1884 |
Total |
11211 |
9134 |
11495 |
13638 |
14251 |
Autres recherches d'anomalie chromosomique par analyse moléculaire (MLPA, QF-PCR, QMPSF...)
D’autres techniques de génétique moléculaire permettent la recherche d’anomalies chromosomiques, notamment : la MLPA (Multiplex ligation-dependent probe amplification), QF-PCR (Quantitative Fluorescence - polymerase chain reaction) et la QMPSF (Quantitative Multiplex PCR of Short Fragments). Une part de ces examens est réalisée dans le contexte de validation d’un autre examen notamment d’une puce. Pour les autres situations elles permettent le plus souvent de poser le diagnostic de maladies qui sont décrites dans la partie relative à la génétique moléculaire. Le nombre de ce type d’examen reste autour de 15 000 depuis plusieurs années (Tableau POSTNATAL10).
Tableau POSTNATAL10. Evolution des autres recherches d’anomalies chromosomiques par analyse moléculaire (MLPA, QF-PCR, QMPSF …)
2010 |
2011 |
2012 |
2013 |
2014 |
|
Autres recherches d'anomalies chromosomiques par analyse moléculaire (MLPA, QF-PCR, QMPSF...) |
12968 |
15553 |
16954 |
14934 |
15079 |
Activité de génétique moléculaire
En 2014, plus de 481 500 examens de génétique moléculaire ont été réalisés en France (Tableau POSTNATAL3). Ils incluaient près de 19 600 examens de pharmacogénétique (4%) (Tableau POSTNATAL18). Au final 397 800 personnes ont bénéficié d’un examen de génétique (plusieurs examens peuvent être réalisés pour une même personne).
Nous avons décidé de baser l’identification des maladies sur la classification de l’encyclopédie Orphanet. Ainsi peuvent être comptabilisées comme deux pathologies distinctes deux formes d’une même maladie enregistrées sous deux numéros ORPHA différents.
Le numéro Orpha est un identifiant unique, stable dans le temps, associé à chaque entité de la classification Orphanet des maladies rares. Ces entités peuvent être des groupes de maladies, des maladies ou des sous-types de maladies. Les numéros Orpha sont destinés, entre autres, à être inclus dans les systèmes d'information en santé afin de permettre l'identification des patients ayant une maladie rare, qu'elle soit génétique ou pas.
Le numéro Orpha désigne des entités cliniques qui peuvent être associés à un ou plusieurs gènes.
Chaque numéro Orpha peut correspondre à un ou plusieurs numéros OMIM.
Génétique des maladies
En 2014, environ 371 135 personnes ont eu un examen de génétique moléculaire, qu’il s’agisse de cas index (personne symptomatique chez qui on fait le diagnostic) ou d’apparentés. Les examens de pharmacogénétique sont présentés dans le chapitre suivant. Les laboratoires français ont développé des examens diagnostiques pour 1 531 maladies différentes (selon la classification Orphanet). Ces maladies étant dans leur grande majorité rares, voir extrêmement rares, 1 333 maladies ont réellement fait l’objet de recherche diagnostique en 2014. Ces examens ont concerné 1 577 gènes différents (Tableau POSTNATAL11).
Deux indications, « hémochromatose » et « thrombophilie non rare » (2 gènes : FII et FV) représentent à elles seules 38,5 % des examens réalisés en 2014 (Tableau POSTNATAL11). Il s’agit des 2 seuls examens de génétique moléculaire répertoriés dans la nomenclature des actes de biologie médicale. Si en volume, ces deux tests sont importants, leur réalisation est peu couteuse et peu chronophage par rapport à l’analyse de gènes complexes.
La liste des 50 examens les plus réalisés en France (Tableau POSTNATAL13) montre la présence de plusieurs maladies pour lesquelles les gènes impliqués sont des gènes de susceptibilité. Une réflexion globale sur l’intérêt de tels examens devra être menée. A titre d’exemple plus de 66 310 (14,5%) examens ont porté sur des gènes du HLA en 2014 (hors indication de greffe). Les laboratoires français ont développé entre 1 et plus de 100 diagnostics de maladies différentes, mais 26,3 % d’entre eux ne proposent qu’un ou deux tests (Tableau POSTNATAL17).
Les maladies génétiques sont très majoritairement rares, voire très rares. Développer des examens diagnostiques pour ces dernières peut se révéler très complexe. Ainsi, les laboratoires se sont généralement spécialisés, 99 laboratoires sont seuls à proposer le diagnostic d’une (ou de plusieurs) maladie(s) en France. Au final, 908 maladies (59 %) ne sont diagnostiquées que dans un seul laboratoire (Tableau POSTNATAL15).
Alors qu’en 2013 seuls 36 laboratoires avaient réalisé des examens en utilisant des appareils permettant des analyses NGS (next generation sequencing), ils ont été 55 à le faire en 2014. Cette augmentation montre la montée en puissance de cette technologie. Une particularité du NGS est la possibilité d’analyser des panels de plusieurs gènes au cours du même examen. Cette évolution des pratiques est suivie par l’Agence de la biomédecine et devrait conduire à une modification à moyen terme du recueil des données dans le cadre du rapport annuel d’activité. En 2014, un peu moins de 17 000 examens de NGS ont été rendus aux prescripteurs soit 3,7% de l’ensemble des examens de génétique moléculaire (hors pharmacogénétique). Cette augmentation du nombre d’examens par NGS est probablement aussi à mettre en regard de la stabilité de l’activité des analyses par puces. En effet, cette approche est souvent comparable à celle des puces (ciblées le plus souvent, mais potentiellement pangénomiques).
Cette évolution des pratiques nécessite que l’on s’assure du maintien de l’exercice en réseau des laboratoires qui individuellement ne pourront développer l’expertise nécessaire à l’interprétation des résultats obtenus sur l’ensemble d’un génome.
Une analyse de niveau 1 consiste en la recherche des mutations les plus fréquentes dont le lien de causalité avec la maladie étudiée est clairement établi. La technique utilisée est généralement simple et souvent basée sur des dispositifs spécifiquement développés pour une recherche ciblée. En conséquence, le résultat d’une analyse de niveau 1 est le plus souvent binaire et toutes les mutations ne sont généralement pas étudiées.
Une analyse de niveau 2 consiste en l’analyse exhaustive du gène, la technique peut être simple ou complexe. Toute technique de balayage pour rechercher des mutations inconnues entre dans ce cadre. Pour ce faire, le laboratoire devra assurer notamment la prise en charge d’échantillons d’autres laboratoires lorsque les analyses de niveau 1 n’ont pas permis de mettre en évidence de mutation et si le contexte clinique le justifie. Il devra également assurer la veille technologique et scientifique, la participation à l’organisation du contrôle de qualité, le lien avec un centre de référence de la maladie s’il existe. Le laboratoire réalisant une analyse de niveau 1 est en relation avec un laboratoire de niveau 2 pour cette même analyse. Il est souhaitable que ce dernier laboratoire soit celui qui organise le contrôle de qualité (Tableau POSTNATAL12). Enfin une analyse de niveau 3 est une analyse de niveau 2 pour laquelle la technique de NGS a été utilisée.
La figure POSTNATAL4 montre la répartition des indications par nombre d’examens pratiqués et illustre la rareté de la majorité des maladies génétiques. En effet, plus d’un tiers des maladies (35,9%) ne sont recherchées au maximum que 10 fois dans l’année et un autre tiers (31,9%) entre 10 et 50 fois.
Le nombre d’examens est plus élevé que le nombre d’individus testés car pour une même maladie l’analyse de plusieurs gènes en parallèle ou successivement peut être nécessaire pour poser un diagnostic.
Tableau POSTNATAL11. Activité de génétique moléculaire postnatale (hors pharmacogénétique)
2010 |
2011 |
2012 |
2013 |
2014 |
|
Nombre de maladies différentes |
. |
. |
. |
. |
. |
Disponibles |
1094 |
1215 |
1369 |
1443 |
1531 |
Réalisés |
958 |
1021 |
1174 |
1252 |
1333 |
Nombre de gènes différents |
. |
. |
. |
. |
. |
Disponibles |
1212 |
1383 |
1495 |
1577 |
1750 |
Réalisés |
1093 |
1215 |
1323 |
1426 |
1577 |
Nombre d'examens réalisés |
350368 |
372422 |
395202 |
404849 |
461936 |
dont hémochromatose type 1 et facteur II facteur V |
135234 |
145164 |
140237 |
163936 |
177846 |
Tableau POSTNATAL12. Nombre d'examens et de laboratoires pour une maladie étudiée par au moins dix laboratoires par génétique moléculaire postnatale en 2014
ORPHA |
Maladie |
Nombre |
Nombre |
Nombre de |
Nombre de |
ORPHA64738 |
Thrombophilie non rare |
70 |
143277 |
69 |
1 |
ORPHA139498 |
Hémochromatose type 1 |
52 |
41612 |
45 |
9 |
ORPHA586 |
Mucoviscidose |
34 |
10482 |
22 |
13 |
ORPHA908 |
Syndrome de l'X fragile |
30 |
10793 |
18 |
12 |
ORPHA1646 |
Délétion partielle du chromosome Y |
28 |
4463 |
23 |
5 |
ORPHA48 |
Absence congénitale bilatérale des canaux déférents |
23 |
545 |
12 |
11 |
ORPHA273 |
Dystrophie myotonique de type 1 |
19 |
1978 |
9 |
10 |
ORPHA825 |
Spondylarthrite ankylosante |
18 |
24531 |
15 |
3 |
ORPHA144 |
Cancer du côlon héréditaire non polyposique |
16 |
4719 |
1 |
16 |
ORPHA145 |
Syndrome héréditaire de prédisposition au cancer du sein et de l'ovaire |
16 |
28290 |
. |
16 |
ORPHA555 |
Maladie coeliaque |
14 |
7417 |
10 |
4 |
ORPHA739 |
Syndrome de Prader-Willi |
14 |
722 |
10 |
4 |
ORPHA117 |
Maladie de Behçet |
13 |
11110 |
10 |
3 |
ORPHA399 |
Maladie de Huntington |
13 |
1141 |
7 |
6 |
ORPHA619 |
Insuffisance ovarienne précoce |
13 |
4897 |
8 |
5 |
ORPHA676 |
Pancréatite chronique héréditaire |
13 |
3013 |
6 |
7 |
ORPHA2073 |
Narcolepsie-cataplexie |
12 |
7705 |
9 |
3 |
ORPHA243377 |
Diabète de type 1 |
12 |
8894 |
8 |
4 |
ORPHA550 |
MELAS |
12 |
956 |
4 |
8 |
ORPHA653 |
Néoplasie endocrinienne multiple type 2 |
11 |
592 |
1 |
10 |
ORPHA70 |
Amyotrophie spinale proximale |
11 |
1836 |
7 |
4 |
ORPHA72 |
Syndrome d'Angelman |
11 |
480 |
9 |
3 |
ORPHA848 |
Bêta-thalassémie |
11 |
710 |
3 |
8 |
ORPHA179 |
Choriorétinopathie type birdshot |
10 |
632 |
7 |
3 |
ORPHA324 |
Maladie de Fabry |
10 |
364 |
. |
10 |
ORPHA357 |
Syndrome de Gilbert |
10 |
851 |
8 |
2 |
ORPHA551 |
MERRF |
10 |
430 |
3 |
7 |
ORPHA778 |
Syndrome de Rett |
10 |
617 |
1 |
9 |
ORPHA90636 |
Surdité neurosensorielle non syndromique autosomique récessive type DFNB |
10 |
2113 |
2 |
10 |
* Analyse de niveau 1 : Recherche des mutations les plus fréquentes dont la causalité pour la maladie étudiée est clairement démontrée. La technique utilisée est généralement simple et souvent basée sur des dispositifs spécifiquement établis pour une recherche ciblée.
Analyse de niveau 2: L’analyse du gène est exhaustive, la technique peut être simple ou complexe. Toute technique de balayage pour rechercher des mutations inconnues rentre dans ce cadre à l’exception des examens réalisés par NGS.
Analyse de niveau 3: Analyse de niveau 2 pour laquelle au moins un résultat positif en NGS a été rendu pour un examen.
Tableau POSTNATAL13. Evolution sur 3 ans de l'activité pour les 50 indications faisant l'objet du plus grand nombre d'examens en 2014
Le tableau complet décrivant l’évolution du nombre d’examens par indication est disponible au format Excel sur le site de l’Agence de la biomédecine
ORPHA |
MALADIE |
2012 |
2013 |
2014 |
ORPHA64738 |
Thrombophilie non rare |
108520 |
131837 |
143277 |
ORPHA139498 |
Hémochromatose type 1 |
38337 |
39633 |
41612 |
ORPHA145 |
Syndrome héréditaire de prédisposition au cancer du sein et de l'ovaire |
20764 |
21921 |
28290 |
ORPHA825 |
Spondylarthrite ankylosante |
33983 |
26667 |
24531 |
ORPHA117 |
Maladie de Behçet* |
26967 |
10885 |
11110 |
ORPHA908 |
Syndrome de l' X fragile |
10003 |
10432 |
10793 |
ORPHA586 |
Mucoviscidose |
11427 |
10253 |
10482 |
ORPHA243377 |
Diabète sucré de type 1 |
7247 |
8583 |
8894 |
ORPHA2073 |
Narcolepsie-Cataplexie |
6582 |
6997 |
7705 |
ORPHA555 |
Maladie coeliaque |
3277 |
3754 |
7417 |
ORPHA155 |
Cardiomyopathie hypertrophique familiale isolée |
1862 |
2372 |
5624 |
ORPHA284130 |
Polyarthrite rhumatoïde |
3131 |
1865 |
5071 |
ORPHA619 |
Insuffisance ovarienne primaire |
628 |
974 |
4897 |
ORPHA552 |
Syndrome MODY |
1420 |
2167 |
4825 |
ORPHA144 |
Cancer du côlon héréditaire non polyposique |
3977 |
4077 |
4719 |
ORPHA1646 |
Délétion partielle de l'Y |
4154 |
4126 |
4463 |
ORPHA29072 |
Pheochromocytome-paragangliome héréditaire |
2239 |
3192 |
3765 |
ORPHA853 |
Thrombopénie materno-foetale et néonatale allo-immune |
263 |
1155 |
3586 |
ORPHA676 |
Pancréatite chronique héréditaire |
2804 |
2553 |
3013 |
ORPHA478 |
Syndrome de Kallmann |
749 |
1181 |
2185 |
ORPHA90636 |
Surdité neurosensorielle non syndromique autosomique récessive type DFNB |
1419 |
1514 |
2113 |
ORPHA273 |
Dystrophie myotonique de type 1 |
2000 |
2034 |
1978 |
ORPHA70 |
Amyotrophie spinale proximale |
1781 |
1859 |
1836 |
ORPHA618 |
Mélanome malin familial |
2070 |
2303 |
1822 |
ORPHA406 |
Hypercholestérolémie familiale |
1761 |
1513 |
1796 |
ORPHA846 |
Alpha-thalassémie |
1293 |
1612 |
1794 |
ORPHA154 |
Cardiomyopathie dilatée familiale isolée |
697 |
510 |
1689 |
ORPHA2512 |
Microcéphalie primaire autosomique récessive |
348 |
649 |
1457 |
ORPHA342 |
Fièvre méditerranéenne familiale |
1261 |
1326 |
1414 |
ORPHA2162 |
Holoprosencéphalie |
479 |
346 |
1404 |
ORPHA98733 |
Syndrome de Noonan et syndrome associé |
. |
. |
1277 |
ORPHA399 |
Maladie de Huntington |
1047 |
1059 |
1141 |
ORPHA803 |
Sclérose latérale amyotrophique |
762 |
951 |
1134 |
ORPHA110 |
Syndrome de Bardet-Biedl |
718 |
712 |
1111 |
ORPHA774 |
Maladie de Rendu-Osler-Weber |
842 |
921 |
1108 |
ORPHA100973 |
Déficit intellectuel FRAXE |
747 |
1236 |
1079 |
ORPHA636 |
Neurofibromatose type 1 |
504 |
606 |
989 |
ORPHA178469 |
Déficit intellectuel autosomique dominant non-syndromique |
10 |
11 |
971 |
ORPHA101016 |
Syndrome de Romano-Ward |
1168 |
1062 |
965 |
ORPHA652 |
Néoplasie endocrinienne multiple type 1 |
951 |
1056 |
965 |
ORPHA550 |
Syndrome MELAS |
893 |
848 |
956 |
ORPHA432 |
Hypogonadisme hypogonadotropique congénital sans anosmie |
676 |
972 |
944 |
ORPHA733 |
Polypose adénomateuse familiale |
761 |
803 |
943 |
ORPHA55 |
Albinisme oculo-cutané |
252 |
188 |
935 |
ORPHA232 |
Drépanocytose |
759 |
894 |
900 |
ORPHA357 |
Syndrome de Gilbert |
421 |
343 |
851 |
ORPHA104 |
Neuropathie optique héréditaire de Leber |
726 |
906 |
849 |
ORPHA262 |
Dystrophie musculaire de Duchenne et Becker |
1141 |
992 |
849 |
ORPHA95698 |
Hyperplasie congénitale des surrénales par déficit en 21-hydroxylase non-classique |
794 |
874 |
838 |
ORPHA558 |
Syndrome de Marfan |
665 |
755 |
833 |
* La variation du nombre d’examens de cette maladie semble être liée à des erreurs de saisie des laboratoires
Tableau POSTNATAL14. Evolution sur 3 ans du nombre de cas rendus positifs pour les 50 indications faisant l'objet du plus grand nombre de cas rendus positifs en 2014
Le tableau complet décrivant l’évolution du nombre de cas rendus positifs par indication est disponible au format Excel sur le site de l’Agence de la biomédecine
ORPHA |
MALADIE |
2012 |
2013 |
2014 |
ORPHA64738 |
Thrombophilie non rare |
7100 |
11457 |
9109 |
ORPHA139498 |
Hémochromatose type 1 |
2525 |
2824 |
2129 |
ORPHA825 |
Spondylarthrite ankylosante |
764 |
2104 |
1210 |
ORPHA145 |
Syndrome héréditaire de prédisposition au cancer du sein et de l'ovaire |
971 |
894 |
1185 |
ORPHA284130 |
Polyarthrite rhumatoïde |
413 |
568 |
720 |
ORPHA846 |
Alpha-thalassémie |
632 |
550 |
638 |
ORPHA232 |
Drépanocytose |
465 |
516 |
614 |
ORPHA555 |
Maladie coeliaque |
152 |
330 |
586 |
ORPHA636 |
Neurofibromatose type 1 |
254 |
337 |
536 |
ORPHA618 |
Mélanome malin familial |
430 |
591 |
426 |
ORPHA586 |
Mucoviscidose |
427 |
358 |
414 |
ORPHA155 |
Cardiomyopathie hypertrophique familiale isolée |
166 |
187 |
406 |
ORPHA117 |
Maladie de Behçet |
152 |
344 |
367 |
ORPHA243377 |
Diabète sucré de type 1 |
60 |
296 |
342 |
ORPHA399 |
Maladie de Huntington |
293 |
326 |
334 |
ORPHA908 |
Syndrome de l' X fragile |
303 |
328 |
333 |
ORPHA98878 |
Hémophilie A |
302 |
288 |
332 |
ORPHA144 |
Cancer du côlon héréditaire non polyposique |
271 |
250 |
320 |
ORPHA2073 |
Narcolepsie-Cataplexie |
225 |
414 |
306 |
ORPHA406 |
Hypercholestérolémie familiale |
273 |
235 |
299 |
ORPHA342 |
Fièvre méditerranéenne familiale |
207 |
254 |
292 |
ORPHA853 |
Thrombopénie materno-foetale et néonatale allo-immune |
134 |
36 |
265 |
ORPHA848 |
Bêta-thalassémie |
343 |
318 |
263 |
ORPHA95698 |
Hyperplasie congénitale des surrénales par déficit en 21-hydroxylase non-classique |
269 |
231 |
257 |
ORPHA273 |
Dystrophie myotonique de type 1 |
308 |
254 |
251 |
ORPHA357 |
Syndrome de Gilbert |
178 |
199 |
231 |
ORPHA90636 |
Surdité neurosensorielle non syndromique autosomique récessive type DFNB |
140 |
138 |
223 |
ORPHA238616 |
Maladie d'Alzheimer |
445 |
337 |
222 |
ORPHA730 |
Polykystose rénale autosomique dominante |
200 |
150 |
218 |
ORPHA676 |
Pancréatite chronique héréditaire |
190 |
167 |
217 |
ORPHA395 |
Homocystinurie par déficit en méthylènetétrahydrofolate réductase |
150 |
246 |
209 |
ORPHA552 |
Syndrome MODY |
166 |
149 |
209 |
ORPHA319681 |
Non-persistence de la lactase à l'âge adulte |
. |
345 |
202 |
ORPHA262 |
Dystrophie musculaire de Duchenne et Becker |
186 |
206 |
200 |
ORPHA558 |
Syndrome de Marfan |
182 |
110 |
194 |
ORPHA745 |
Thrombophilie héréditaire due au déficit congénital en protéine C |
169 |
144 |
190 |
ORPHA774 |
Maladie de Rendu-Osler-Weber |
157 |
139 |
176 |
ORPHA903 |
Maladie de Von Willebrand |
160 |
90 |
163 |
ORPHA827 |
Maladie de Stargardt |
54 |
56 |
158 |
ORPHA619 |
Insuffisance ovarienne primaire |
26 |
26 |
157 |
ORPHA362 |
Déficit en glucose-6-phosphate déshydrogénase |
114 |
102 |
156 |
ORPHA29072 |
Pheochromocytome-paragangliome héréditaire |
127 |
121 |
151 |
ORPHA48 |
Absence congénitale bilatérale des canaux déférents |
121 |
87 |
146 |
ORPHA269 |
Dystrophie facio-scapulo-humérale |
107 |
161 |
144 |
ORPHA805 |
Sclérose tubéreuse de Bourneville |
141 |
167 |
141 |
ORPHA55 |
Albinisme oculo-cutané |
59 |
56 |
136 |
ORPHA70 |
Amyotrophie spinale proximale |
140 |
120 |
136 |
ORPHA358 |
Syndrome de Gitelman |
92 |
94 |
132 |
ORPHA640 |
Neuropathie héréditaire avec hypersensibilité à la pression |
148 |
115 |
130 |
ORPHA60 |
Déficit en alpha-1 antitrypsine |
104 |
141 |
126 |
Figure POSTNATAL4. Répartition des maladies par nombre d'examens réalisés en 2014
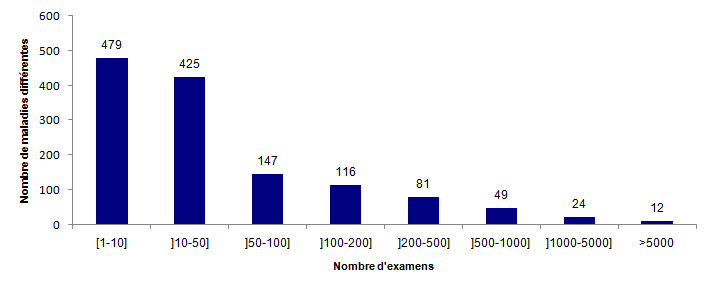
Tableau POSTNATAL15. Description de l'activité de génétique moléculaire postnatale
2010 |
2011 |
2012 |
2013 |
2014 |
|
Nombre de laboratoires |
|
|
|
|
|
qui n'étudient que l'hémochromatose type 1 et facteur II facteur V |
25 |
21 |
20 |
19 |
18 |
qui n'étudient que la thrombophilie |
22 |
17 |
18 |
16 |
16 |
Nombre de laboratoires |
|
|
|
|
|
qui diagnostiquent une maladie qui n'est étudiée que dans 1 laboratoire en France |
97 |
100 |
100 |
98 |
99 |
qui diagnostiquent une maladie qui n'est étudiée que dans 2 laboratoires en France |
94 |
97 |
102 |
95 |
99 |
Nombre de maladies |
|
|
|
|
|
qui ne sont étudiées que dans 1 laboratoire en France |
673 |
739 |
832 |
885 |
908 |
qui ne sont étudiées que dans 2 laboratoires en France |
222 |
239 |
280 |
305 |
343 |
Tableau POSTNATAL16. Evolution de l'activité de diagnostic à la suite d’un dépistage néonatal de la mucoviscidose
2011 |
2012 |
2013 |
2014 |
|
Nombre de laboratoires ayant eu une activité de diagnostic à la suite d’un dépistage néonatal de la mucoviscidose |
9 |
8 |
8 |
10 |
Nombre de nouveaux nés analysés |
3231 |
3430 |
3145 |
2890 |
Nombre de cas positifs rendus (2 mutations) |
154 |
92 |
73 |
137 |
Tableau POSTNATAL17. Evolution du pourcentage de laboratoires selon le nombre de diagnostics de génétique moléculaire proposés
Nombre de diagnostics de génétique moléculaire proposés |
Laboratoires |
|||||||||
2010 |
2011 |
2012 |
2013 |
2014 |
||||||
N |
% |
N |
% |
N |
% |
N |
% |
N |
% |
|
1 à 2 |
57 |
32,9 |
57 |
32,2 |
51 |
29,3 |
53 |
29,6 |
46 |
26,3 |
3 à 10 |
57 |
32,9 |
55 |
31,1 |
53 |
30,5 |
58 |
32,4 |
59 |
33,7 |
11 à 20 |
22 |
12,7 |
28 |
15,8 |
30 |
17,2 |
26 |
14,5 |
27 |
15,4 |
21 à 35 |
24 |
13,9 |
22 |
12,4 |
21 |
12,1 |
22 |
12,3 |
22 |
12,6 |
36 à 100 |
12 |
6,9 |
14 |
7,9 |
18 |
10,3 |
19 |
10,6 |
19 |
10,9 |
> 100 |
1 |
0,6 |
1 |
0,6 |
1 |
0,6 |
1 |
0,6 |
2 |
1,1 |
Total |
173 |
100,0 |
177 |
100,0 |
174 |
100,0 |
179 |
100,0 |
175 |
100,0 |
Activité de pharmacogénétique
La pharmacogénétique est l’étude du lien entre certaines caractéristiques génétiques constitutionnelles d’un individu et la réponse de l’organisme à un ou des médicaments. En 2014, 16 663 individus ont bénéficié d’un examen de pharmacogénétique et 53 laboratoires ont eu une activité de pharmacogénétique.
Une augmentation continue du nombre d’examens de pharmacogénétique réalisés par les laboratoires est observée entre 2010 et 2013 (Tableau POSTNATAL18). En 2014 le nombre d’examens réalisés diminue par rapport à l’année précédente avec 19 596 analyses. Cette diminution est très probablement liée à une modification majeure du recueil de l’activité. En effet, la classification utilisée les années précédentes a évolué pour avoir des données plus précises. Ainsi les situations où une même analyse pouvait être comptabilisée plusieurs fois par un laboratoire ont été quasiment supprimées.
Un travail continu est réalisé sur ce recueil afin de poursuivre l’amélioration de l’information. Il est primordial que les laboratoires soient en mesure de connaître l’indication pour laquelle ils réalisent un examen lorsqu’il peut y en avoir plusieurs (cas ou un même gène pourrait être impliqué dans plusieurs indications).
On peut observer que la réalisation d’examens « toxicité de l’abacavir » qui était en continuelle augmentation semble atteindre un plateau en 2014 (Tableau POSTNATAL20). La modification du recueil n’impacte pas cette indication, ni celle de la réponse au traitement anti-viral dans l'hépatite C (gène IL28B) qui voit son nombre d’examens chuter de près de moitié (48,3%) entre 2013 et 2014 alors qu’il était en croissance depuis 2010. Pour ce dernier examen, la diminution de nombre de réalisations est directement liée à la diminution de la prescription du médicament pour lequel était fait ce test. Il devrait disparaitre avec l’apparition de nouveaux traitements de l’hépatite C.
Tableau POSTNATAL18 Evolution de l'activité de pharmacogénétique
2010 |
2011 |
2012 |
2013 |
2014* |
|
Nombre d'examens réalisés |
10800 |
15737 |
20425 |
25303 |
19596 |
Nombre de laboratoires avec activité de pharmacogénétique |
31 |
35 |
44 |
47 |
53 |
Nombre de laboratoires ayant uniquement pratiqué une activité de pharmacogénétique |
4 |
3 |
5 |
5 |
5 |
* Une modification de la classification des indications de pharmacogénétique a été réalisée en 2014. Cette modification impacte le recueil de l’activité. Toute comparaison avec les années précédentes doit prendre en compte ce paramètre.
Tableau POSTNATAL19. Examens de pharmacogénétique effectués en 2014
ORPHA |
Indications* de l'examen |
Nombre |
Nombre de |
Nombre de |
Nombre de |
ORPHA240841 |
Toxicité de l'abacavir |
6707 |
8 |
6 |
14 |
ORPHA240839 |
Toxicité des dérivés du fluorouracile |
3387 |
6 |
2 |
8 |
ORPHA284102 |
Réponse au traitement anti-viral dans l'hépatite C |
2215 |
22 |
2 |
24 |
ORPHA413687 |
Surdosage ou adaptation de dose de l'azathioprine ou 6-mercaptopurine |
2091 |
16 |
2 |
18 |
ORPHA240885 |
Toxicité de l'irinotécan |
1784 |
12 |
1 |
13 |
ORPHA241043 |
Adaptation posologique du tacrolimus |
1720 |
10 |
1 |
11 |
ORPHA413674 |
Surdosage ou adaptation de dose des AVK |
678 |
8 |
3 |
10 |
ORPHA413667 |
Surdosage ou adaptation posologique des anti dépresseurs ou antipsychotiques |
614 |
3 |
3 |
6 |
ORPHA240935 |
Résistance au clopidogrel |
84 |
2 |
1 |
3 |
ORPHA240869 |
Toxicité de l'efavirenz |
80 |
2 |
3 |
5 |
ORPHA413690 |
Surdosage ou adaptation de dose du méthotrexate |
44 |
4 |
1 |
5 |
ORPHA240863 |
Toxicité du cisplatine |
43 |
2 |
. |
2 |
ORPHA413684 |
Résistance aux AVK |
37 |
2 |
4 |
6 |
ORPHA240921 |
Toxicité du voriconazole |
29 |
2 |
2 |
4 |
ORPHA284121 |
Toxicité / non réponse clozapine |
22 |
1 |
1 |
2 |
ORPHA240887 |
Toxicité de l'isoniazide |
19 |
1 |
1 |
2 |
ORPHA413693 |
Toxicité des curarisants |
11 |
. |
2 |
2 |
ORPHA240947 |
Résistance au tamoxifène |
4 |
1 |
1 |
2 |
ORPHA413696 |
Toxicité des statines (inhibiteurs HMG CoA) |
3 |
. |
1 |
1 |
ORPHA240867 |
Toxicité de la codéine |
1 |
1 |
. |
1 |
ORPHA240905 |
Toxicité du raltégavir |
1 |
. |
1 |
1 |
ORPHA413681 |
Surdosage ou adaptation de dose des hypoglycémiants oraux (sulf et glinides) |
1 |
. |
1 |
1 |
* Indications répertoriées dans la classification Orphanet
Tableau POSTNATAL20. Evolution selon l'indication du prélèvement du nombre d'examens de pharmacogénétique
ORPHA |
Indication* de l'examen |
2010 |
2011 |
2012 |
2013 |
2014 |
ORPHA240839 |
Toxicité des dérivés du fluorouracile |
2190 |
2442 |
3871 |
3643 |
3387 |
ORPHA240841 |
Toxicité de l'abacavir |
1918 |
3395 |
3900 |
6417 |
6707 |
ORPHA240863 |
Toxicité du cisplatine |
. |
. |
. |
586 |
43 |
ORPHA240867 |
Toxicité de la codéine |
. |
. |
. |
48 |
1 |
ORPHA240869 |
Toxicité de l'efavirenz |
4 |
505 |
60 |
83 |
80 |
ORPHA240885 |
Toxicité de l'irinotécan |
1919 |
1757 |
1996 |
2283 |
1784 |
ORPHA240887 |
Toxicité de l'isoniazide |
2 |
27 |
55 |
40 |
19 |
ORPHA240905 |
Toxicité du raltégavir |
1 |
3 |
. |
37 |
1 |
ORPHA240921 |
Toxicité du voriconazole |
. |
6 |
9 |
24 |
29 |
ORPHA240935 |
Résistance au clopidogrel |
19 |
90 |
106 |
124 |
84 |
ORPHA240947 |
Résistance au tamoxifène |
27 |
64 |
12 |
48 |
4 |
ORPHA241017 |
Susceptibilité à l'ictère dans le traitement par le raltegravir |
2 |
4 |
4 |
299 |
. |
ORPHA241043 |
Adaptation posologique du tacrolimus |
672 |
1103 |
1829 |
1351 |
1720 |
ORPHA284102 |
Réponse au traitement anti-viral dans l'hépatite C |
475 |
3339 |
4292 |
4287 |
2215 |
ORPHA284121 |
Toxicité / non réponse clozapine |
. |
1 |
2 |
12 |
22 |
ORPHA413667 |
Surdosage ou adaptation posologique des anti dépresseurs ou antipsychotiques |
48 |
366 |
436 |
1373 |
614 |
ORPHA413674 |
Surdosage ou adaptation de dose des AVK |
230 |
209 |
622 |
519 |
678 |
ORPHA413681 |
Surdosage ou adaptation de dose des hypoglycémiants oraux (sulf et glinides) |
. |
. |
29 |
190 |
1 |
ORPHA413684 |
Résistance aux AVK |
165 |
81 |
138 |
115 |
37 |
ORPHA413687 |
Surdosage ou adaptation de dose de l'azathioprine ou 6-mercaptopurine |
1034 |
1515 |
2257 |
3084 |
2091 |
ORPHA413690 |
Surdosage ou adaptation de dose du méthotrexate |
104 |
137 |
61 |
94 |
44 |
ORPHA413693 |
Toxicité des curarisants |
30 |
26 |
144 |
228 |
11 |
ORPHA413696 |
Toxicité des statines (inhibiteurs HMG CoA) |
15 |
86 |
181 |
42 |
3 |
* Indications répertoriées dans la classification Orphanet